Konfigurasi makromolekul dan stereoisomer. Konformasi dan fleksibilitas makromolekul
Klasifikasi polimer menurut struktur kimia rantai utama dan makromolekul secara keseluruhan. Interaksi antarmolekul dalam polimer. Konsep kepadatan energi kohesi dan parameter kelarutan.
Struktur makromolekul meliputi struktur kimia dan panjangnya, distribusi panjang dan berat molekul, bentuk dan penataan ruang satuan. Berdasarkan struktur kimia rantai utama, mereka dibedakan rantai homo (dengan rantai atom karbon - rantai karbon ) Dan heterorantai polimer, dan menurut struktur kimia makromolekul secara keseluruhan - polimer:
· organik - rantai terdiri dari atom karbon, oksigen, nitrogen dan belerang;
· elemen organo - rantai terdiri dari silikon, fosfor dan atom lain yang terikat atom atau gugus karbon, atau sebaliknya;
· anorganik - sama sekali tidak ada atom karbon atau atom rantai karbon dengan ikatan rangkap dua atau rangkap tiga tanpa gugus samping.
Paling umum rantai karbon organik polimer, termasuk berbagai turunannya (mengandung halogen, eter, alkohol, asam, dll.), yang namanya dibentuk dari nama monomer dengan awalan “poli”. Polimer rantai karbon alifatik jenuh antara lain polietilen, polipropilen, polivinil klorida, politetrafluoroetilen, politrifluorokloroetilen, polivinil alkohol, polivinil asetat, poliakrilamida, poliakrilonitril, polimetil metakrilat dan lain-lain. Tak jenuh adalah polibutadiena, poliisoprena dan polikloroprena, contoh polimer aromatik lemak adalah polietilenfenilena, dan polimer aromatik adalah polifenilen. Nomor homochain anorganik polimer terbatas - karbin rantai karbon (~C≡C-C≡C~) dan kumulena (=C=C=C=), serta polisulfur (~S-S-S~), polisilana (~SiH 2 -SiH 2 ~), poligerman (~GeH 2 -GeH 2 ~), dll. Lebih umum homochain organoelemen polimer yang terbuat dari rantai organik (rantai karbo) dengan gugus samping organoelemen atau dari rantai anorganik dengan radikal organik: polivinilalkilsilan, poliorganosilan, polimer yang mengandung boron. Heterochain organik Polimer dibagi menjadi beberapa kelas tergantung pada sifat gugus fungsi dalam rantai utama. Mereka dapat bersifat alifatik atau aromatik, tergantung pada struktur gugus hidrokarbon antar gugus fungsi (Tabel 1.1).
Tabel 1.1.
Polimer heterochain dari berbagai kelas:
| Kelompok fungsional | Polimer | |
| Nama kelas | Perwakilan | |
| Mengandung oksigen | ||
| Sederhana dan halus | Polieter | Polimetilen oksida (~CH 2 -O~) |
| Polietilen oksida (~CH 2 -CH 2 -O~) | ||
| Ester | Poliester | Polietilen tereftalat ([-CH 2 -CH 2 -O-OC-Ar-CO-O-] n) |
| Poliarilat ([-OC-R-COO-R`-O-] n) | ||
| Polikarbonat ([-O-Ar-CH 2 -Ar-O-CO-O-Ar-CH 2 -Ar-] n) | ||
| Mengandung nitrogen | ||
| asetal | Asetal | Selulosa (C 6 H 1 0 O 5) n |
| Amida | Poliamida (-СО-NN-) | Adipamid poliheksametilen |
| imida | Polimida | Polipiromellitimida |
| Urea | poliurea | Polinonametilen urea |
| Uretan | Poliuretan (–HN-CO-O) | ~(CH 2) 4 -O-CO-NH-(CH 2) 2 ~ |
| Mengandung belerang | ||
| Thioester | Polisulfida | Polietilen sulfida (~CH 2 -CH 2 -S~) |
| Sulfonik | Polisulfon | Poli- N,N`-oksidifenilsulfon |
Heterochain anorganik polimer adalah poliborazol, asam polisilat, polifosfonitril klorida. Heterochain organoelemen polimer mencakup sekelompok besar senyawa paling populer dari rantai anorganik dengan gugus samping organik. Ini termasuk polimer yang mengandung silikon, yang rantainya terdiri dari atom silikon dan oksigen bergantian ( poliorganosiloksan ) atau nitrogen ( poliorganosilazan ). Polimer dengan heteroatom ketiga di rantai utama - logam - disebut polimetalorganosiloksan (polialuminium organosiloksan, poliboron organosiloksan, dan polititanium organosiloksan). Ada juga polimer dengan rantai organoanorganik karbon, silikon, atom oksigen (polikarbosiloksan, polikarbosilan, polikarboran), yang mungkin mengandung unit alifatik atau aromatik. Semua atom dalam ikatan polimer yang dipertimbangkan terhubung ikatan kovalen kimia . ada juga koordinasi (khelat, intrakompleks) polimer heterochain yang unit-unitnya dihubungkan melalui interaksi donor-akseptor dengan pembentukan ion logam tautan koordinasi (valensi samping) dan ikatan ionik (valensi utama). Ikatan kimia dan logam dengan panjang 0,1-0,2 nm secara signifikan melebihi nilai energi ikatan fisik dan bahkan ikatan hidrogen (panjang 0,24-0,32 nm), yang menempati posisi perantara antara ikatan fisik dan kimia. Polaritas ikatan juga bergantung pada struktur kimia dan komposisi satuan, yang diukur dengan nilai momen dipol μ HAI, sama dengan produk muatan dan jarak antar muatan (Tabel 1.3), serta tingkat interaksi antarmolekul dalam polimer. Tergantung pada polaritas ikatannya, polimer dapat berupa kutub Dan non-polar . Momen dipol semua polimer alifatik rantai karbon organik (non-polar) mendekati nol. Tergantung pada struktur makromolekul, dispersi, orientasi dan ikatan induktif dapat muncul di antara mereka. Dispersif ikatan disebabkan oleh munculnya dipol sesaat pada atom ketika elektron berputar mengelilingi inti. Makromolekul polar dicirikan oleh orientasi hubungan (dipol-dipol). Di bidang dipol makromolekul polar, makromolekul nonpolar juga dapat terpolarisasi. Antara dipol permanen dan terinduksi, induksi komunikasi.
Interaksi antarmolekul menentukan kemampuan polimer untuk larut dalam cairan dengan berat molekul rendah, perilaku pada suhu rendah, sifat elastis dan lainnya. Levelnya diukur parameter kelarutan – rasio produk kerapatan polimer dengan jumlah konstanta tarikan masing-masing kelompok atom dalam suatu unit komposit dengan berat molekul unit tersebut. Untuk ini mereka juga menggunakan kepadatan energi kohesi (kJ/mol), yang setara dengan usaha menghilangkan makromolekul atau kelompok atom yang berinteraksi satu sama lain pada jarak yang sangat jauh. Pada suhu transisi gelas T s energi interaksi antarmolekul menjadi lebih tinggi daripada energi gerak termal, dan polimer masuk ke dalam keadaan vitrifikasi padat . Polimer dengan T Dengan diatas suhu kamar disebut plastik , dan di bawah suhu kamar dan parameter kelarutan adalah 14-19 ( M . J/m 3 ) 1/2 – elastomer (karet).
Berat molekul polimer dan metode penentuannya. Distribusi massa molekul dan bentuk makromolekul. Klasifikasi polimer menurut jumlah dan urutan susunan unit penyusunnya.
Massa molekul(MM) adalah karakteristik penting dari struktur polimer, menentukan tingkat sifat mekanik dan termasuk dalam kelompok tertentu: oligomer (termoset) - 10 3 -10 4, termoplastik kristal - 10 4 -5 . 10 4, termoplastik amorf - 5 . 10 4 -2 . 10 5, karet – 10 5 -10 6. Semakin rendah MM polimer, semakin rendah viskositas lelehannya dan semakin mudah pembentukannya. Sifat mekanik lebih ditentukan oleh derajat pengerasan (oligomer) dan kristalinitas (poliamida, poliester) atau transisi ke keadaan seperti kaca. MM tertinggi adalah karet yang sulit dibentuk, namun produk berbahan karet tersebut memiliki elastisitas yang tinggi. Karena MW yang besar tidak menghasilkan tingkat polimerisasi yang sama, ukuran makromolekul berbeda. Polidispersitas (polimolekulalitas) adalah salah satu konsep dasar kimia fisika polimer, dan jenisnya distribusi berat molekul (MWD) merupakan indikator penting yang mempengaruhi sifat fisik dan mekanik polimer tidak kurang dari MM.
Karena MM adalah nilai statistik rata-rata, metode penentuannya yang berbeda memberikan nilai yang berbeda. DENGAN angka yang jarang Metode ini didasarkan pada penentuan jumlah makromolekul dalam larutan polimer encer, misalnya dengan mengukur tekanan osmotiknya, dan massa rata-rata - untuk menentukan massa makromolekul, misalnya dengan mengukur hamburan cahaya. Angka rata-rata MM ( M N ) diperoleh hanya dengan membagi massa sampel polimer dengan jumlah makromolekul di dalamnya, dan rata-rata massa MM: M w =M 1 w 1 +M 2 w 2 +…+M i wi , Di mana w 1 , w 2 , dengan saya – pecahan massa pecahan; M 1 , M 2 , saya – pecahan MM rata-rata massa. Viskositas rata-rata MM, yang mendekati MM rata-rata massa, ditentukan oleh viskositas larutan encer. Polimer disebut monodispersi , jika terdiri dari satu fraksi dengan ukuran makromolekul yang sangat berdekatan, dan untuk itu perbandingannya Mw/M N =1,02-1,05. Dalam kasus lain, rata-rata massa MM lebih besar dari jumlah rata-rata MM, dan rasionya ( Mw/M N =2.0-5.0) adalah ukuran polidispersitas polimer. Lebih Mw/M N , semakin luas MMRnya. Pada kurva MWD polimer, nilainya M N menyumbang maksimum, yaitu. menjadi fraksi yang bagiannya dalam komposisi polimer paling besar, dan Mw bergeser ke kanan sepanjang sumbu x.
Besarnya ukuran makromolekul polimer menentukan ciri lain dari strukturnya. Mereka bisa menjadi linier atau bercabang (dengan cabang samping dari rantai utama atau berbentuk bintang). Pada nilai MM dekat mereka menjadi isomer . Sifat-sifat polimer yang terdiri dari makromolekul linier dan bercabang sangat bervariasi. Percabangan - indikator yang tidak diinginkan dari struktur makromolekul, mengurangi keteraturannya dan mempersulit kristalisasi polimer. Koneksi makromolekul melalui ikatan kimia mengarah pada pembentukan struktur jaring , selanjutnya mengubah sifat polimer. Sesuai dengan perbedaan struktur makromolekul (Gbr. 1.1), polimer disebut linier , bercabang Dan jaring (dijahitkan ).
Dalam kasus terakhir, konsep “makromolekul” kehilangan maknanya, karena seluruh sampel polimer yang berikatan silang menjadi satu molekul raksasa. Oleh karena itu, dalam polimer ikatan silang, nilai rata-rata MM segmen rantai antara ikatan kimia (simpul jaringan) yang menghubungkan makromolekul ditentukan.
Kopolimer mengandung unit dua atau lebih monomer berbeda dalam rantai utama (misalnya, karet stirena-butadiena) dan memiliki struktur yang lebih kompleks daripada homopolimer , terdiri dari unit satu monomer. Kopolimer dengan kombinasi acak unit monomer dalam makromolekul disebut statistik , dengan pergantian yang benar - bergantian , dan dengan sebagian besar bagian (blok) unit satu monomer - blok kopolimer . Jika blok salah satu monomer menempel pada rantai utama suatu makromolekul, yang tersusun dari unit-unit monomer lain, dalam bentuk cabang samping yang besar, maka kopolimer disebut divaksinasi . Struktur kopolimer dicirikan oleh komposisi kimia dan panjang blok atau rantai cangkokan serta jumlah blok atau cangkokan dalam makromolekul. Unit monomer yang sama atau berbeda dapat dihubungkan secara teratur (akhir dari satu - awal dari yang lain) atau tidak teratur (akhir dari satu adalah akhir dari yang lain, awal dari yang lain adalah awal dari tautan ketiga, dll.), dan substituen dalam kelompok samping dapat memiliki susunan spasial yang teratur atau tidak teratur. Struktur makromolekul juga ditentukan oleh konfigurasi dan konformasinya.
Konfigurasi makromolekul dan stereoisomer. Konformasi dan fleksibilitas makromolekul. Polimer rantai fleksibel dan kaku serta bentuk makromolekulnya.
Konfigurasi makromolekul- ini adalah susunan spasial tertentu dari atom-atomnya, yang tidak berubah selama pergerakan termal, akibatnya berbagai jenisnya merupakan isomer stabil. isomer Cis ditandai dengan letak substituen yang berbeda pada sisi ikatan rangkap yang berbeda pada setiap unit berulang, dan isomer trans - adanya substituen berbeda pada satu sisi ikatan rangkap. Contoh isomer tersebut adalah NA dan gutta-percha - poliisoprena alami yang struktur kimianya identik. Gutta-percha adalah plastik dengan struktur kristal yang meleleh pada suhu 50-70 °C, dan NK adalah elastomer pada kisaran suhu +100 HAI Dari ke -72 HAI C, karena makromolekulnya berbeda periode identitas . DI DALAM cis-Gugus metil poliisoprena (NC) yang berorientasi satu arah terjadi melalui satu satuan penyusun yaitu sebesar 0,82 nm, dan dalam miliknya kesurupan-isomer (gutta-percha) – setelah 0,48 nm:
cis- 1,4-poliisoprena (NC)
kesurupan-1.4-poliisoprena
Dari makromolekul polimer optik dengan atom karbon asimetris, metode sintesis khusus digunakan untuk memperolehnya isomer stereoregular - isotaktik (substituen berada pada satu sisi bidang makromolekul) dan sindiotaktik (deputi berada di sisi yang berlawanan):
Sifatnya berbeda dari ataktik polimer dengan susunan substituen yang tidak beraturan. Tolak-menolak timbal balik dari substituen menyebabkan perpindahannya relatif satu sama lain dalam ruang, dan oleh karena itu bidang simetri melengkung dalam bentuk spiral. Struktur spiral juga merupakan karakteristik polimer yang aktif secara biologis (misalnya, heliks ganda DNA). Struktur makromolekul stereoisomer adalah pembawa informasi tentang metode sintesisnya, dan dalam protein, heliks ganda DNA membawa banyak informasi tentang keturunan biologisnya.
Konformasi makromolekul- ini adalah susunan spasial atom atau kelompok atom, yang dapat berubah di bawah pengaruh gerakan termal tanpa merusak ikatan kimia di antara mereka. Besarnya panjang makromolekul, dengan kemungkinan rotasi bagian-bagiannya di sekitar ikatan kimia tetap, menentukan isomer rotasi , dinyatakan dalam munculnya konformasi yang berbeda. Semakin dekat atom hidrogen satu sama lain ( cis-posisi), semakin besar tolakannya dan, karenanya, energi potensial makromolekul. Interaksi ditingkatkan oleh substituen polar, seperti atom klor. DI DALAM kesurupan-isomer, energi potensial makromolekul lebih kecil, susunan atom lebih menguntungkan daripada di cis-isomer. Energi penghalang rotasi bagian dari makromolekul yang membuatnya terhambat , terdiri dari serangkaian osilasi, membantu mengatasinya fluktuasi energi panas . Himpunan osilasi dan gerakan di sekitar sambungan sederhana mengarah ke ke kelengkungan makromolekul di ruang angkasa, yang dapat bergerak ke berbagai arah dan berubah seiring waktu. Dengan kata lain, makromolekul memiliki fleksibilitas - kemampuan untuk mengubah konformasinya sebagai akibat dari pergerakan termal atau aksi kekuatan eksternal. Dengan jumlah atom yang banyak, rantai tidak hanya dapat menekuk, tetapi juga genap menggulung sangat longgar kumparan makromolekul , yang ukurannya dapat dikarakterisasi akar rata-rata jarak kuadrat antara ujung-ujungnya dan menghitung secara matematis, mengetahui jumlah link penyusun di dalamnya. Karena adanya struktur rantai makromolekul, maka pergerakan suatu atom atau gugus akan menyebabkan pergerakan atom atau gugus lainnya, sehingga timbullah gerakan yang mirip dengan gerakan ulat atau cacing, yang disebut ulangan (Gbr. 1.2). Bagian dari suatu rantai yang bergerak secara keseluruhan dalam suatu gerak dasar disebut segmen rantai . Fleksibilitas termodinamika mencirikan kemampuan rantai untuk mengubah konformasi di bawah pengaruh gerakan termal dan dapat dinilai dengan parameter kekakuan, panjang segmen termodinamika, atau parameter fleksibilitas Flory. Semakin rendah indikator ini, semakin tinggi kemungkinan suatu makromolekul berpindah dari satu konformasi ke konformasi lainnya (Tabel 1.4). Parameter kekerasan diperkirakan dengan rasio jarak akar rata-rata kuadrat antara ujung rantai nyata dan rantai yang disambung bebas dalam larutan polimer encer. Panjang segmen termodinamika A (Segmen Kuhn) mencirikan urutan tautan di mana setiap tautan berperilaku independen satu sama lain, dan juga terkait dengan jarak akar-rata-rata-kuadrat antara ujung-ujung rantai. Ini sama dengan panjang hidrodinamik makromolekul untuk rantai yang sangat kaku dan panjang unit berulang untuk rantai yang sangat fleksibel. Polimer dari seri diena dan dengan ikatan ~Si-O~ atau ~C-O~ pada rantai utama dicirikan oleh fleksibilitas yang lebih besar dibandingkan dengan polimer dari seri vinil, karena penurunan interaksi pertukaran antara CH 2 -Grup memiliki energi isomer putar 100 kali lebih rendah. Sifat substituen mempunyai pengaruh yang kecil terhadap fleksibilitas makromolekul. Parameter fleksibilitas Flory F HAI menunjukkan kandungan ikatan fleksibel dalam makromolekul dan berfungsi sebagai kriteria fleksibilitas yang membagi polimer rantai fleksibel (F HAI>0,63; A<10nm) Dan rantai kaku (F HAI<0,63; A>35nm). Yang terakhir tidak dalam konformasi kumparan makromolekul dan memiliki bentuk makromolekul memanjang - tali elastis (polialkil isosianat, A =100), poros engkol (poli- P-benzamid, A =210) atau spiral (biopolimer, A =240).Fleksibilitas kinetik makromolekul mencerminkan laju transisinya dalam medan gaya dari satu konformasi ke konformasi lainnya dan ditentukan oleh nilainya segmen kinetik , yaitu. bagian dari makromolekul yang merespons pengaruh eksternal secara keseluruhan. Berbeda dengan segmen termodinamika, segmen ini ditentukan oleh suhu dan kecepatan pengaruh eksternal. Dengan meningkatnya suhu, energi kinetik dan fleksibilitas makromolekul meningkat dan ukuran segmen kinetik berkurang. Dalam kondisi di mana waktu kerja gaya lebih besar daripada waktu transisi dari satu konformasi ke konformasi lainnya, fleksibilitas kinetiknya tinggi, dan besarnya segmen kinetik mendekati segmen termodinamika. Selama deformasi yang cepat, segmen kinetik mendekati panjang hidrodinamik makromolekul, dan bahkan rantai yang fleksibel secara termodinamika berperilaku seperti rantai kaku. Fleksibilitas kinetik makromolekul terisolasi ditentukan dari sifat viskoelastik larutan yang sangat encer, diikuti dengan ekstrapolasi hingga konsentrasi nol. Makromolekul dari polimer amorf rantai fleksibel memiliki berbentuk bola baik dalam bentuk terisolasi maupun dalam jumlah besar. Selain itu, struktur polimer tidak mirip dengan struktur “molekul terasa”, di mana makromolekul terjerat secara kacau, seperti yang diperkirakan sebelumnya. Gagasan daerah terurut dalam polimer amorf diungkapkan pada tahun 1948 oleh Alfrey.
konfigurasi makromolekul jika tidak struktur primer(Bahasa inggris) - susunan spasial atom dalam . Ditentukan oleh nilai sudut ikatan dan panjang ikatan yang bersesuaian.
Keterangan
Konfigurasi makromolekul ditentukan oleh posisi relatif unit monomer penyusunnya, serta strukturnya. Saat ini, istilah “struktur” atau “struktur primer” biasanya digunakan untuk menggambarkan konfigurasi makromolekul.
Perbedaan dibuat antara tatanan konfigurasi jarak pendek (konfigurasi perlekatan unit-unit tetangga) dan jarak jauh, yang mencirikan struktur bagian makromolekul yang cukup luas. Ukuran kuantitatif dari kebijaksanaan (keteraturan) adalah tingkat stereoregularitas. Selain itu, taktik dapat digambarkan dengan jumlah berbagai jenis pasangan tetangga terdekat (di-, tri-, tetrad), yang distribusinya ditentukan secara eksperimental. Karakteristik kuantitatif dari konfigurasi makromolekul jaringan statistik, misalnya, adalah kepadatan ikatan silang, yaitu bagian rata-rata rantai antar node jaringan.
Konfigurasi makromolekul ditentukan oleh analisis difraksi sinar-X, birefringence, dll. Biasanya, setiap metode paling “sensitif” terhadap karakteristik konfigurasi apa pun; Jadi, NMR dalam banyak kasus memungkinkan untuk mengkarakterisasi urutan konfigurasi jarak pendek secara kuantitatif
· polimer organik(komposisinya mencakup unsur organogenik - C, N, O, P, S). Mereka dibagi menjadi homochain (rantai utama hanya mengandung atom karbon) dan heterochain (rantai utama mencakup atom lain). Kelas polimer ini termasuk biopolimer.
· polimer organoelemen(dalam rantai utama, bersama dengan atom karbon, terdapat atom Si, Al, Ti, Ge, B).
· polimer anorganik ( rantai utama tidak mengandung atom karbon, seperti silikon).
1. Sebutkan jenis-jenis tata nama polimer.
2. Bagaimana tata nama berdasarkan nama monomer terbentuk?
3. Berikan contoh nama polimer dengan menggunakan tata nama berdasarkan struktur kimia rantai polimer.
4. Sebutkan jenis-jenis klasifikasi polimer. Berikan contoh.
5. Jenis kopolimer apa saja yang ada?
6. Bagaimana klasifikasi kimia polimer dilakukan?
Masalah untuk solusi mandiri*
2. Klasifikasi dan rumus struktur polimer utama
2.1 Klasifikasi polimer
Soal 2501 – 2502, 2403 – 2406, 2307
2.2. Rumus struktur polimer utama
Soal 3501, 3402, 3303 – 3309
*Berikut ini tugas-tugas yang diberikan dari “Kumpulan tugas tes untuk penguasaan tematik dan akhir pada disiplin ilmu “Kimia dan Fisika Polimer”, M., MITHT, 2009.
Bagian No.3. Ciri-ciri utama makromolekul
Makromolekul dicirikan oleh 4 parameter utama:
1. Berat molekul (MM), distribusi massa molekul (MWD);
2. Konfigurasi makromolekul;
3. Konformasi makromolekul;
4. Topologi (linier, bercabang).
· MM memungkinkan Anda menentukan panjang dan ukuran makromolekul;
· Konfigurasi menentukan struktur kimia makromolekul;
· Konformasi menentukan bentuk makromolekul.
3.1. Berat molekul (MM), distribusi berat molekul (MWD)
Perbedaan utama antara konsep MM untuk IUD dan NMS:
MW adalah ukuran panjang molekul untuk polimer linier dan dapat dinyatakan dalam MW unit berulang penyusun berbobot molekul rendah:
https://pandia.ru/text/78/135/images/image040_18.gif" width="12" height="2 src=">m0 – berat molekul unit berulang senyawa;
Pn – derajat polimerisasi
Kebanyakan polimer sintetik bukanlah senyawa individual, tetapi terdiri dari campuran molekul dengan ukuran berbeda tetapi komposisinya sama.
Hal ini mengarah pada:
· untuk polimer, berat molekul efektif adalah nilai rata-rata karena polidispersitas - penyebaran makromolekul berdasarkan berat molekul;
· untuk sebagian besar polimer, kelompok ujung berbeda dari komposisi ikatan dalam rantai polimer;
· Cabang samping tertentu mungkin ada pada makromolekul, hal ini juga membedakan makromolekul satu sama lain;
· sebagian besar biopolimer merupakan senyawa individual (setiap polimer spesifik memiliki komposisi, struktur, dan berat molekul yang unik).
Alasan polidispersitas:
1. karena sifat statistik dari proses produksi polimer: selama proses sintesis, makromolekul dengan berbagai panjang diperoleh;
2. karena proses penghancuran sebagian makromolekul, misalnya selama pengoperasian material;
3. karena perbedaan kelompok ujung molekul polimer;
4. karena beberapa polimer memiliki cabang di tempat berbeda dan struktur kimia berbeda.
3.1.1. Metode untuk merata-ratakan massa molekul
1) Rata-rata atas jumlah molekul
Jumlah rata-rata MM:
w=∑(Ni Mi2)/∑(NiMi) (3.1.1.2)
Massa fraksi dari berat molekul tertentu diperhitungkan.
Mw ditentukan dengan menggunakan metode kromatografi, ultrasentrifugasi, dan hamburan cahaya.
Kn=Mw/Mn (3.1.1.3)
Untuk polimer monodisperse (biologis) Kn=1.
Dengan distribusi sempit Kn=1,01±1,05.
Dalam industri, polimer dengan Kn=3±10 paling sering diproduksi.
3) Viskositas rata-rata mm:
Mŋ=((∑NiMi)1+α/∑(NiMi))1/α, 0<α<1 (3.1.1.4)
![]()
3.1.2. Distribusi massa molekul (MWD)
Ciri berat molekul polimer yang paling lengkap adalah fungsi distribusi berat molekul.
Nitrogen, boron, dan aluminium dapat menjadi elemen rantai makromolekul pada komponen lain struktur polimer, atau dimasukkan sebagai heteroatom dalam rantai utama.

4.3. Karbon
Ia mempunyai kecenderungan yang tinggi untuk membentuk ikatan kovalen yang kuat, baik antara atomnya sendiri maupun dengan atom lain.
https://pandia.ru/text/78/135/images/image064_12.gif" width="102" height="92"> - struktur karbon-karbon dua dimensi dari graphene, grafit, dan jelaga
Dimungkinkan juga untuk memperoleh rantai linier atom karbon:
https://pandia.ru/text/78/135/images/image066_10.gif" width="238" height="14 src=">
Saat dipanaskan, berubah menjadi grafit.
Peluang yang jauh lebih besar untuk membangun makromolekul linier dari atom karbon terbuka ketika 1 atau 2 valensi karbon jenuh dengan atom atau gugus lain.
 - polietilen
- polietilen
 - polipropilen
- polipropilen
![]() - politetrafluoroetilen
- politetrafluoroetilen
Selain itu, rantai utama mungkin berisi berbagai kelompok yang mengandung heteroatom:
https://pandia.ru/text/78/135/images/image071_11.gif" width="93" height="43 src="> - grup ester
https://pandia.ru/text/78/135/images/image073_9.gif" width="105" height="45 src="> - golongan karbamid (urea)
https://pandia.ru/text/78/135/images/image076_9.gif" width="185 height=84" height="84">
Tapi silikon tidak terlalu stabil secara kimia dan selama oksidasi, silikon berikatan dengan oksigen, membentuk ikatan silikon-oksigen yang sangat kuat.
Di alam, silikon terdapat dalam bentuk kuarsa:

Ini adalah struktur tiga dimensi kaku yang tidak menunjukkan sifat “polimer” makromolekul linier. Makromolekul linier diperoleh dengan mengganti dua valensi setiap atom silikon dengan radikal organik (CH3-, C2H5-, dll). Dalam hal ini, polimer silikon-organik muncul.
Polimer yang mengandung silikon dapat disintesis:
 - polisiloksan
- polisiloksan
Atom Al, B, Ti, Zn dan beberapa lainnya dapat dibangun menjadi rantai.
4.5. Fosfor
Atom fosfor dapat membentuk polimer, tetapi rantai utama juga harus mencakup atom lain (paling sering oksigen):
 - polifosfat
- polifosfat
 - asam polifosfat
- asam polifosfat
Residu asam ortofosfat ditemukan dalam polimer alami (asam nukleat, DNA dan RNA):

Jadi, atom divalen atau polivalen (C, O, P, N, S, Si, Al, B dan lain-lain) dapat berupa unsur rantai utama makromolekul atau terletak pada fragmen samping; atom monovalen (H, F, Cl, J, Br dan beberapa lainnya) hanya dapat tersusun sebagai substituen.
Kimia polimer dibangun berdasarkan unsur-unsur ini.
4.6. Jenis polimer
Polimer diperoleh baik secara sintetis, atau diekstraksi dari organisme hidup (biopolimer), atau dengan mengolah polimer alami yang sudah diisolasi.
Beberapa polimer yang dibuat secara sintetis ada di alam. Polimer diperoleh dari monomer - zat dengan berat molekul rendah atau sebagai hasil transformasi polimer jadi (sintetis atau alami) - transformasi analog polimer.

1,4-cis-polibutadiena tidak ada di alam; ia diperoleh secara sintetis dari butadiena.

1,4-cis-poliisoprena ada di alam (karet alam), tetapi disintesis di alam dari glukosa dan zat lain (tetapi tidak dari isoprena, seperti di industri)

Poliester ini dapat diperoleh dengan kondensasi poli-β-hidroksibutirat, dan pada saat yang sama juga disintesis oleh sejumlah bakteri.
Sintesis biopolimer tidak akan dibahas dalam kursus ini.
Banyak polimer alami yang sangat sulit diproduksi secara sintetik. Mereka diproduksi pada organisme hidup sebagai hasil reaksi biokimia yang kompleks.
Polimer alami yang paling penting:
Contohnya termasuk reaksi poliesterifikasi:
HO-R-COOH + HO-R-COOH > HO-R-COO-R-COOH + H2O, dst.
poliamidasi:
H2N-R-NH2 + ClOC-R"-COCl > H2N-R-NHCO-R"-COCl + HCl, dst.
Selain itu, berbeda dengan polimerisasi, komposisi unsur produk polikondensasi dalam hal ini tidak sesuai dengan komposisi senyawa monomer, karena setiap tindakan kimia polikondensasi disertai dengan pelepasan molekul produk dengan berat molekul rendah.
Skema umum polikondensasi di atas juga berhubungan dengan beberapa jenis proses yang tidak disertai dengan pelepasan produk dengan berat molekul rendah. Ini termasuk, misalnya, sintesis poliuretan dari glikol dan diisosianat:
HO-R-OH + O=C=N-R"-N=C=O > HO-R-O-CO-NH-R"-N=C=O, dst.
Proses polikondensasi seperti ini sering disebut politambahan. Menurut hukum kinetik, reaksi poliadisi sangat mirip dengan reaksi polikondensasi. Pada kedua jenis proses polikondensasi, pertumbuhan makromolekul dilakukan melalui interaksi gugus fungsi molekul monomer atau gugus yang sama yang terletak di ujung rantai yang sudah terbentuk dengan berat molekul berbeda. Produk antara polimer yang diperoleh dari reaksi ini cukup stabil dan dapat diisolasi dalam bentuk bebas. Namun, mereka mengandung gugus reaktif di ujungnya dan oleh karena itu mampu melakukan reaksi kondensasi lebih lanjut, baik satu sama lain maupun dengan molekul monomer yang sesuai. Oleh karena itu, secara teoritis, polikondensasi dapat dianggap selesai hanya jika semua gugus fungsi terminal bereaksi, menghasilkan pembentukan satu makromolekul siklik raksasa. Namun dalam praktiknya, hal ini tidak pernah tercapai.
Pertanyaan untuk belajar mandiri:
1. Unsur Tabel Periodik manakah yang mampu membentuk rantai polimer?
2. Berikan contoh polimer yang dihasilkan secara sintetik.
3. Berikan contoh polimer alam.
4. Monomer apa yang dapat berpartisipasi dalam reaksi polimerisasi?
1.3. Konfigurasi makromolekul
Konsep konfigurasi mencakup susunan spasial tertentu dari atom makromolekul, yang tidak berubah selama pergerakan termal. Transisi dari satu konfigurasi ke konfigurasi lainnya tidak mungkin terjadi tanpa memutus ikatan kimia.
Yaitu: 1) konfigurasi tautan, 2) tatanan jarak pendek - konfigurasi tautan penghubung, 3) tatanan jarak jauh - konfigurasi bagian besar (misalnya, balok dan pergantiannya, atau panjang dan sebaran cabang) , 5) konfigurasi rantai memanjang secara keseluruhan.
Konfigurasi tautan. Contohnya adalah konfigurasi cis dan trans dari polimer diena
1,4-cis-poliisoprena 1,4-trans-poliisoprena (karet alam) (gutta-percha) Contoh lainnya adalah l,d-isomerisme. Misalnya,
untuk polimer dengan unit ~CH2 –CHR~, dimana R adalah radikal apa pun, pembentukan dua isomer dimungkinkan: l – levorotatory, dan d – dextrorotatory
Konfigurasi koneksi tautan(urutan jarak pendek). Tautan dalam rantai dapat dihubungkan menggunakan tipe “head to tail” atau “head to head”:

adalah koneksi head-to-tail, dan koneksi head-to-head memerlukan mengatasi hambatan aktivasi yang besar.
Untuk kopolimer, jenis isomer strukturnya lebih banyak dibandingkan dengan homopolimer. Misalnya, untuk kopolimer butadiena dan stirena, hal ini dimungkinkan:
1. pergantian tautan yang berurutan –A–B–A–B–A–B–,
2. kombinasi tautan dalam bentuk angka dua dan tiga serangkai–AA–BBV–AA–BBV– ,
3. kombinasi statistik tautan–AA–B–AA–BBB–A–B– . Urutan konfigurasi jarak jauh menyebar
puluhan dan ratusan atom dalam rantai utama. Misalnya, rangkaian besar blok dalam kopolimer blok atau rangkaian besar unit dengan stereoregularitas yang sama (misalnya, polimer dengan struktur isotaktik, ataktik, dan sindiotaktik).
Sindiotaktik Ataktik Isotaktik
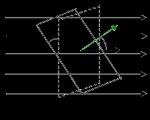
Konfigurasi sirkuit keseluruhan ditentukan oleh susunan timbal balik dari rangkaian tautan yang besar (dengan tatanan jangka panjang). Misalnya, untuk makromolekul bercabang, berbagai jenis konfigurasi ditunjukkan pada Gambar 4.
Beras. 4. Konfigurasi makromolekul

1.4. Konformasi makromolekul
Konformasi adalah distribusi variabel dalam ruang atom atau kelompok atom yang membentuk makromolekul. Peralihan dari satu konformasi ke konformasi lainnya dapat terjadi karena adanya rotasi, perputaran atau getaran satuan-satuan di sekitar ikatan tunggal di bawah pengaruh gerak termal atau gaya luar dan tidak disertai dengan putusnya ikatan kimia.
Polimer dapat mempunyai konformasi yang berbeda:
Bola statistik adalah konformasi terlipat. Terbentuk ketika intensitas pergerakan termal internal melebihi pengaruh eksternal. Karakteristik polimer linier [PE, PP, PB, PIB dan polimer tangga (polifenilen siloksan).
Heliks – terbentuk dalam polimer karena ikatan H (misalnya, dalam molekul protein dan asam nukleat).
Globule adalah partikel yang bentuknya sangat kompak, mendekati bola. Karakteristik polimer dengan interaksi intramolekul yang kuat (misalnya PTFE).
Batang atau tali ditemukan dalam alkil poliisosianat.
Lipat konformasi. Karakteristik polimer dalam keadaan kristal (misalnya PE).
Konformasi Poros Engkol direalisasikan dalam poli-n-benzenamida.
Gambar.5. Konformasi makromolekul
1.5. Fleksibilitas makromolekul
Fleksibilitas adalah salah satu karakteristik polimer yang paling penting, yang menentukan sifat sangat elastis, relaksasi dan termomekanik polimer, serta sifat larutannya. Fleksibilitas mencirikan kemampuan makromolekul untuk mengubah bentuknya di bawah pengaruh pergerakan termal ikatan atau pengaruh mekanis eksternal. Fleksibilitas disebabkan oleh rotasi internal tautan atau bagian makromolekul relatif satu sama lain. Mari kita perhatikan fenomena rotasi internal dalam molekul menggunakan contoh senyawa organik paling sederhana - molekul etana.
Dalam molekul etana (CH3 –CH3), atom karbon terikat dengan atom hidrogen dan satu sama lain melalui ikatan kovalen (ikatan σ), dan sudut antara arah ikatan σ (sudut ikatan) adalah 1090 28/. Hal ini menyebabkan susunan substituen (atom hidrogen) tetrahedral dalam ruang dalam molekul etana. Karena gerakan termal dalam molekul etana, satu gugus CH3 berputar relatif terhadap gugus lainnya di sekitar sumbu C-C. Dalam hal ini, susunan spasial atom dan energi potensial molekul terus berubah. Secara grafis, berbagai susunan ekstrim atom dalam suatu molekul dapat direpresentasikan dalam bentuk proyeksi molekul pada bidang horizontal (Gbr. 6). Misalkan pada posisi a energi potensial molekul sama dengan U1, dan pada posisi b – U2, sedangkan U1 ≠ U2, yaitu. posisi molekul tidak seimbang secara energi. Posisi b, di mana atom-atom H terletak di bawah satu sama lain, secara energetik tidak menguntungkan, karena gaya tolak-menolak muncul di antara atom-atom H, yang cenderung memindahkan atom-atom ke posisi yang secara energetik menguntungkan a. Jika kita menerima
U1 =0, lalu U2 =maks.

Beras. 6. Rumus proyeksi letak ekstrim atom H dalam ruang dalam molekul etana.
Beras. 7. Ketergantungan energi potensial suatu molekul pada sudut rotasi gugus metil.
Ketika satu gugus CH3 berotasi 600 relatif terhadap gugus lainnya, molekul berpindah dari posisi a ke b dan kemudian setelah 600 lagi ke posisi a, dan seterusnya. Perubahan energi potensial molekul etana tergantung pada sudut rotasi ditunjukkan pada Gambar 7. Molekul dengan simetri yang lebih kecil (misalnya, molekul dikloroetana) memiliki hubungan yang lebih kompleks U=f(φ).
Potensi (U 0 ) atau rotasi penghalang aktivasi
tion adalah energi yang diperlukan untuk transisi suatu molekul dari posisi minimum ke posisi energi potensial maksimum. Untuk etana, U0 kecil (U0 = 11,7 kJ/mol) dan pada
Pada suhu normal, gugus CH3 berputar mengelilingi ikatan C-C dengan kecepatan tinggi (1010 rpm).
Jika suatu molekul mempunyai cadangan energi kurang dari U0, maka tidak terjadi rotasi dan hanya terjadi getaran atom relatif terhadap posisi energi minimum - hal ini terbatas atau
putaran lambat.
Dalam polimer, karena interaksi intra dan antarmolekul, ketergantungan U=f(φ) memiliki bentuk yang kompleks.
Jika salah satu posisi suatu mata rantai dicirikan oleh energi potensial U1, dan posisi lainnya oleh U2, maka energi transisi dari satu posisi ke posisi lain sama dengan selisih ∆U= U1 – U2. Perbedaan energi transisi ∆U dari satu posisi kesetimbangan suatu unit makromolekul ke unit makromolekul lainnya menjadi ciri khasnya fleksibilitas termodinamika. Ini menentukan kemampuan rantai untuk menekuk di bawah pengaruh gerakan termal.
Karakteristik lain dari fleksibilitas adalah kecepatan peralihan tautan dari satu posisi ke posisi lain. Laju transformasi konformasi bergantung pada rasio nilai U0 dan energi pengaruh luar. Semakin besar U0, semakin lambat putaran link dan semakin sedikit fleksibilitasnya. Fleksibilitas makromolekul yang ditentukan oleh nilai U0 disebut fleksibel kinetik
Faktor penentu fleksibilitas makromolekul
Faktor-faktor tersebut meliputi: nilai U0, massa molekul polimer, kepadatan jaringan spasial, ukuran substituen dan suhu.
Penghalang rotasi potensial (U 0). Nilai U0 tergantung pada interaksi intra dan antarmolekul. Mari kita perhatikan faktor-faktor yang mempengaruhi U0 dan fleksibilitas rantai dalam polimer rantai karbon.
Polimer rantai karbon
Dalam polimer rantai karbon, hidrokarbon jenuh adalah yang paling polar. Interaksi intra dan antarmolekulnya kecil, dan nilai U0 dan ∆U kecil, sehingga polimer memiliki fleksibilitas kinetik dan termodinamika yang besar. Contoh: PE, PP, PIB.
Nilai U0 sangat rendah terutama untuk polimer yang rantainya terdapat ikatan rangkap di sebelah ikatan tunggal.
–CH2 –CH=CH–CH2 – Polibutadiena Pengenalan ke dalam makromolekul substituen yang mengandung
kelompok polar menyebabkan interaksi intra dan antarmolekul. Dalam hal ini, derajat polaritas berpengaruh signifikan
Saat memperkenalkan kelompok kutub, ada tiga kemungkinan dampak pada fleksibilitas:
1. Kelompok kutub letaknya berdekatan dan interaksi yang kuat mungkin terjadi di antara mereka. Transisi polimer tersebut dari satu posisi spasial ke posisi spasial lainnya memerlukan mengatasi U0 yang besar, oleh karena itu rantai polimer tersebut adalah yang paling tidak fleksibel.
2. Gugus polar jarang terdapat dalam suatu rantai dan interaksi di antara mereka tidak muncul. Nilai U0 dan ∆U kecil dan polimer memiliki fleksibilitas kinetik dan termodinamika yang lebih besar.

–СF 2 –СF 2 –
Contoh: Polikloroprena
3. Kelompok kutub disusun sedemikian rupa sehingga medan listrik saling menghilangkan. Dalam hal ini, momen dipol total makromolekul sama dengan nol. Oleh karena itu, nilai U0 dan ∆U rendah dan polimer memiliki fleksibilitas kinetik dan termodinamika yang lebih besar.
Contoh: Politetrafluoroetilen
Polimer rantai hetero
Dalam polimer heterochain, rotasi dimungkinkan di sekitar ikatan C–O, C–N, Si–O, dan C–C. Nilai U0 untuk ikatan ini kecil dan rantainya memiliki fleksibilitas kinetik yang cukup. Contoh: poliester, poliamida, poliuretan, karet silikon.
Namun, fleksibilitas polimer heterochain mungkin dibatasi oleh interaksi antarmolekul akibat pembentukan ikatan H (misalnya selulosa, poliamida). Selulosa adalah salah satu polimer rantai kaku. Ini mengandung sejumlah besar gugus polar (–OH) dan oleh karena itu selulosa dicirikan oleh interaksi intra dan antarmolekul, nilai U0 yang tinggi dan fleksibilitas yang rendah.
Berat molekul polimer. Meningkatkan berat molekul polimer meningkatkan pelipatan rantai dan makromolekul yang panjang
memiliki fleksibilitas kinetik yang lebih besar dibandingkan dengan makromolekul pendek. Ketika MW meningkat, jumlah konformasi yang dapat diambil oleh makromolekul meningkat dan fleksibilitas rantai meningkat.
Kepadatan jaringan spasial. Semakin banyak ikatan kimia antar makromolekul, semakin sedikit fleksibilitas rantainya, yaitu. Ketika kepadatan jaringan spasial meningkat, fleksibilitas menurun. Contohnya adalah penurunan fleksibilitas rantai dengan bertambahnya jumlah crosslink pada seri resol< резитол<резит.
Pengaruh ukuran dan jumlah substituen. Peningkatan jumlah substituen polar dan besar mengurangi mobilitas unit makromolekul dan mengurangi fleksibilitas kinetik. Contohnya adalah penurunan fleksibilitas makromolekul kopolimer butadiena dan stirena dengan peningkatan kandungan substituen fenil besar dalam rantai.
Jika terdapat dua substituen pada satu atom karbon dalam tulang punggung polimer (misalnya OCH3 dan CH3 dalam unit PMMA), maka makromolekul menjadi kaku secara kinetik.
Suhu. Dengan meningkatnya suhu, energi kinetik makromolekul meningkat. Selama nilai energi kinetiknya kurang dari U0, rantai akan mengalami getaran puntir. Ketika energi kinetik makromolekul menjadi sama dengan atau melebihi nilai U0, ikatan mulai berputar. Dengan meningkatnya suhu, nilai U0 sedikit berubah, tetapi kecepatan putaran tautan meningkat dan fleksibilitas kinetik meningkat.
Pertanyaan kontrol
1 Informasi umum tentang polimer, konsep, definisi.
2 Jelaskan dan berikan contoh bahan organik, non-
polimer organik dan organoelemen.
2 Klasifikasi polimer homochain, contoh.
3 Klasifikasi polimer heterochain, contoh.
4 Fleksibilitas termodinamika dan kinetik makromolekul. Faktor apa saja yang mempengaruhi fleksibilitas makromolekul?
5 Apa konfigurasi makromolekul dan apa saja kemungkinan jenis konfigurasi makromolekul? Contoh.
6 Apa yang dimaksud dengan konformasi makromolekul dan jenis konformasi makromolekul apa yang mungkin terjadi? Contoh.
7 Parameter apa yang menjadi ciri berat molekul, distribusi berat molekul dan polidispersitas polimer?
8 Karakteristik molekul oligomer.
9 Fraksinasi polimer dan konstruksi kurva molekul distribusi massa kuler.
Dalam konfigurasi tertentu, makromolekul memiliki sejumlah besar derajat kebebasan internal yang terkait dengan rotasi di sekitar sumbu ikatan tunggal rantai utama. Akibatnya, makromolekul mampu mengambil berbagai bentuk ( konformasi), yaitu Polimer dicirikan oleh isomerisme konformasi.
Konformasi adalah susunan spasial atom dan gugus atom, yang dapat diubah tanpa memutus ikatan kimia yang penting sebagai akibat dari pergerakan termal dan (atau) pengaruh eksternal.
Di bawah ini adalah diagram skema mekanisme perubahan konformasi triad isotaktik polimer vinil sebagai akibat dari rotasi 180° di sekitar ikatan C-C. Jelaslah bahwa transisi konformasi seperti itu tidak disertai dengan perubahan konfigurasi dan pemutusan ikatan kimia.
Dengan demikian, Isomerisme konformasi makromolekul ditentukan oleh rotasi internal di sekitar ikatan kimia tunggal dari struktur rantai polimer.
Prinsip dasar isomerisme konformasi makromolekul
Mari kita perhatikan pola dasar rotasi internal di sekitar ikatan kimia menggunakan contoh model molekul rendah - 1,2-dikloroetana.

Karena interaksi substituen samping (Hi C1) dengan rotasi penuh di sekitar sumbu ikatan -C-C sebesar 360°, sejumlah isomer putar yang berbeda secara berurutan diwujudkan dalam molekul 1,2-dikloroetana, atau konformer, dengan energi potensial tertentu. Secara grafis, hal ini dapat direpresentasikan dalam bentuk peta energi - ketergantungan energi potensial konformer pada sudut rotasi. Untuk 1,2-dikloroetana, peta serupa ditunjukkan secara skematis pada Gambar. 1.3.

Beras. 1.3. Ketergantungan energi potensial kamu atom valensi tidak terikat dari molekul 1,2-dikloroetana pada sudut rotasi
Molekul jenis ini memiliki tiga konformasi stabil: satu kesurupan- dan dua konformasi gauche (dari bahasa Perancis. kurang ajar- miring, miring), sesuai dengan minimum kurva potensial. Maksimum tersebut berhubungan dengan konformasi gerhana yang tidak stabil, khususnya konformer r^is.
Dalam polimer, rotasi internal di sekitar ikatan tunggal memiliki sejumlah ciri khusus dibandingkan dengan senyawa dengan berat molekul rendah. Mari kita perhatikan sebuah fragmen rantai polivinil klorida dalam konfigurasi “head-to-head”.

Berbeda dengan 1,2-dikloroetana, dalam fragmen terisolasi, alih-alih dua atom II, substituen pada atom karbon merupakan kelanjutan dari rantai polimer -CH 2 -. Dengan kata lain, ketika berputar di sekitar ikatan antara atom karbon ke-g dan (g+1), atom karbon (g+2) dengan kelanjutan rantai selanjutnya berperan sebagai substituen (Gbr. 1.4).

Beras. 1.4.
Posisi atom (r + 2) relatif terhadap ikatan sebelumnya ditentukan oleh alas kerucut, dengan memperhitungkan sudut ikatan 0. Namun, rotasi 360° hanya mungkin terjadi bila perpanjangan kelanjutan dari ikatan sebelumnya rantai bergerak di ruang angkasa, yang membutuhkan energi panas yang sangat besar, yang biasanya melebihi energi disosiasi senyawa kimia. Akibatnya terjadi rotasi internal pada polimer terhambat dan diimplementasikan dalam busur lingkaran tertentu. Besar kecilnya busur ini menentukan sudut rotasi internal terhambat F. Besarnya sudut rotasi internal yang terhambat bergantung pada suhu, sifat ikatan kimia, polaritas dan volume substituen, komposisi konfigurasi polimer, dll.
Jadi, pada perkiraan pertama, rotasi internal dalam rantai polimer direduksi menjadi rotasi setiap ikatan berikutnya relatif terhadap ikatan sebelumnya. Pada kenyataannya, peristiwa-peristiwa ini memiliki karakter kerja sama yang nyata, karena rotasi dua ikatan yang bertetangga relatif satu sama lain sangat ditentukan oleh proses serupa dalam lingkungan dekat dan interaksi jangka panjang. Dalam hal ini, dalam kasus polimer, sudut rotasi internal yang dihambat adalah nilai rata-rata. Perkiraan kuantitatif dari karakteristik ini akan diberikan di bawah ini.