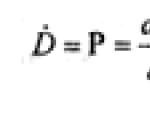कौन सा तत्व. रासायनिक तत्व
रासायनिक अभिक्रियाओं में एक पदार्थ दूसरे में परिवर्तित हो जाता है। यह कैसे होता है यह समझने के लिए, आपको प्राकृतिक इतिहास और भौतिकी के पाठ्यक्रम से यह याद रखना होगा कि पदार्थ परमाणुओं से बने होते हैं। परमाणुओं के प्रकार सीमित संख्या में होते हैं। परमाणु विभिन्न तरीकों से एक दूसरे से जुड़े हो सकते हैं। जिस प्रकार वर्णमाला के अक्षरों को एक साथ जोड़ने पर सैकड़ों-हजारों अलग-अलग शब्द बनते हैं, उसी प्रकार एक ही परमाणु से विभिन्न पदार्थों के अणु या क्रिस्टल बनते हैं।
परमाणु अणु बना सकते हैं- किसी पदार्थ के सबसे छोटे कण जो उसके गुणों को बरकरार रखते हैं। उदाहरण के लिए, ऐसे कई पदार्थ ज्ञात हैं जो केवल दो प्रकार के परमाणुओं - ऑक्सीजन परमाणु और हाइड्रोजन परमाणु, लेकिन विभिन्न प्रकार के अणुओं से बनते हैं। इन पदार्थों में पानी, हाइड्रोजन और ऑक्सीजन शामिल हैं। पानी के अणु में तीन कण एक दूसरे से जुड़े होते हैं। यही तो परमाणु हैं.
ऑक्सीजन परमाणु से (रसायन विज्ञान में ऑक्सीजन परमाणुओं को अक्षर O से दर्शाया जाता है) दो हाइड्रोजन परमाणु जुड़े होते हैं (उन्हें अक्षर H से दर्शाया जाता है)।
एक ऑक्सीजन अणु दो ऑक्सीजन परमाणुओं से बना होता है; एक हाइड्रोजन अणु दो हाइड्रोजन परमाणुओं से बना होता है। अणु रासायनिक परिवर्तनों के दौरान बन सकते हैं, या वे क्षय हो सकते हैं। इस प्रकार, प्रत्येक पानी का अणु दो हाइड्रोजन परमाणुओं और एक ऑक्सीजन परमाणु में टूट जाता है। पानी के दो अणु दोगुने हाइड्रोजन और ऑक्सीजन परमाणु बनाते हैं।
नए पदार्थों के अणु बनाने के लिए समान परमाणु जोड़े में बंधते हैं- हाइड्रोजन और ऑक्सीजन. इस प्रकार अणु नष्ट हो जाते हैं, जबकि परमाणु संरक्षित रहते हैं। यहीं से "परमाणु" शब्द आया, जिसका अनुवाद प्राचीन ग्रीक से किया गया है "अविभाज्य"।
परमाणु पदार्थ के सबसे छोटे रासायनिक रूप से अविभाज्य कण हैं।
रासायनिक परिवर्तनों में, अन्य पदार्थ उन्हीं परमाणुओं से बनते हैं जिनसे मूल पदार्थ बने हैं। जैसे सूक्ष्मदर्शी के आविष्कार से सूक्ष्म जीव अवलोकन के लिए सुलभ हो गए, वैसे ही परमाणु और अणु ऐसे उपकरणों के आविष्कार के साथ सुलभ हो गए जो और भी अधिक आवर्धन देते हैं और यहां तक कि परमाणुओं और अणुओं की तस्वीरें खींचने की भी अनुमति देते हैं। ऐसी तस्वीरों में परमाणु धुंधले धब्बों की तरह दिखते हैं और अणु ऐसे धब्बों के संयोजन की तरह दिखते हैं। हालाँकि, ऐसी घटनाएँ भी होती हैं जिनमें परमाणु विभाजित होते हैं, एक प्रकार के परमाणु दूसरे प्रकार के परमाणु में बदल जाते हैं। इसी समय, कृत्रिम रूप से प्राप्त और ऐसे परमाणु जो प्रकृति में नहीं पाए जाते हैं। लेकिन इन घटनाओं का अध्ययन रसायन विज्ञान द्वारा नहीं, बल्कि एक अन्य विज्ञान - परमाणु भौतिकी द्वारा किया जाता है। जैसा कि पहले ही उल्लेख किया गया है, अन्य पदार्थ भी हैं, जिनमें हाइड्रोजन और ऑक्सीजन परमाणु शामिल हैं। लेकिन, चाहे ये परमाणु पानी के अणुओं की संरचना में शामिल हों, या अन्य पदार्थों की संरचना में, ये एक ही रासायनिक तत्व के परमाणु हैं।
रासायनिक तत्व एक विशिष्ट प्रकार का परमाणु होता है परमाणु कितने प्रकार के होते हैं?आज तक, एक व्यक्ति 118 प्रकार के परमाणुओं, यानी 118 रासायनिक तत्वों के अस्तित्व के बारे में विश्वसनीय रूप से जानता है। इनमें से 90 प्रकार के परमाणु प्रकृति में पाए जाते हैं, बाकी प्रयोगशालाओं में कृत्रिम रूप से प्राप्त किए जाते हैं।
रासायनिक तत्वों के प्रतीक
रसायन विज्ञान में, रासायनिक तत्वों को नामित करने के लिए रासायनिक प्रतीकों का उपयोग किया जाता है। यह रसायन शास्त्र की भाषा है. किसी भी भाषा में भाषण को समझने के लिए, आपको उसी तरह रसायन शास्त्र में अक्षरों को जानना होगा। पदार्थों के गुणों और उनके साथ होने वाले परिवर्तनों को समझने और उनका वर्णन करने के लिए सबसे पहले रासायनिक तत्वों के प्रतीकों को जानना आवश्यक है। कीमिया के युग में, रासायनिक तत्वों को अब की तुलना में बहुत कम जाना जाता था। कीमियागरों ने उनकी पहचान ग्रहों, विभिन्न जानवरों, प्राचीन देवताओं से की। वर्तमान में, स्वीडिश रसायनज्ञ जॉन्स जैकब बर्ज़ेलियस द्वारा प्रस्तुत नोटेशन का उपयोग पूरी दुनिया में किया जाता है। उनकी प्रणाली में, रासायनिक तत्वों को किसी दिए गए तत्व के लैटिन नाम के प्रारंभिक या बाद के अक्षरों में से एक द्वारा दर्शाया जाता है। उदाहरण के लिए, चांदी तत्व को प्रतीक द्वारा दर्शाया गया है - एजी (अव्य। अर्जेंटीना)।नीचे प्रतीकों, प्रतीकों के उच्चारण और सबसे आम रासायनिक तत्वों के नाम दिए गए हैं। उन्हें याद रखने की जरूरत है!
रूसी रसायनज्ञ दिमित्री इवानोविच मेंडेलीव रासायनिक तत्वों की विविधता का आदेश देने वाले पहले व्यक्ति थे, और उन्होंने आवधिक कानून की खोज के आधार पर रासायनिक तत्वों की आवर्त सारणी संकलित की। रासायनिक तत्वों की आवर्त सारणी कैसे व्यवस्थित की जाती है? चित्र 58 आवधिक प्रणाली का एक लघु अवधि संस्करण दिखाता है। आवर्त प्रणाली में ऊर्ध्वाधर स्तंभ और क्षैतिज पंक्तियाँ होती हैं। क्षैतिज रेखाओं को आवर्त कहा जाता है। आज तक, सभी ज्ञात तत्वों को सात आवर्तों में रखा गया है।
अवधियों को 1 से 7 तक अरबी अंकों द्वारा निर्दिष्ट किया जाता है। आवर्त 1-3 में तत्वों की एक पंक्ति होती है - उन्हें छोटा कहा जाता है।
आवर्त 4-7 में तत्वों की दो पंक्तियाँ होती हैं, उन्हें बड़े कहा जाता है। आवर्त सारणी के ऊर्ध्वाधर स्तंभों को तत्वों का समूह कहा जाता है।
कुल मिलाकर आठ समूह हैं, और उन्हें निर्दिष्ट करने के लिए I से VIII तक के रोमन अंकों का उपयोग किया जाता है।
मुख्य और द्वितीयक उपसमूह आवंटित करें। आवधिक प्रणाली- रसायनज्ञ की एक सार्वभौमिक संदर्भ पुस्तक, इसकी सहायता से आप रासायनिक तत्वों के बारे में जानकारी प्राप्त कर सकते हैं। एक अन्य प्रकार की आवर्त प्रणाली है - लंबी अवधि।आवर्त सारणी के दीर्घ आवर्त रूप में तत्वों को अलग-अलग प्रकार से समूहित किया गया है और उन्हें 18 समूहों में बाँटा गया है।
सामयिकप्रणालीतत्वों को "परिवारों" द्वारा समूहीकृत किया जाता है, अर्थात, तत्वों के प्रत्येक समूह में समान, समान गुणों वाले तत्व होते हैं। इस वैरिएंट में आवधिक प्रणाली, समूह संख्याएं, साथ ही अवधि, अरबी अंकों द्वारा दर्शायी जाती हैं। रासायनिक तत्वों की आवधिक प्रणाली डी.आई. मेंडलीव
प्रकृति में रासायनिक तत्वों की व्यापकता
प्रकृति में पाए जाने वाले तत्वों के परमाणु इसमें बहुत ही असमान रूप से वितरित होते हैं। अंतरिक्ष में, सबसे आम तत्व हाइड्रोजन है, जो आवर्त सारणी में पहला तत्व है। यह ब्रह्मांड के सभी परमाणुओं का लगभग 93% हिस्सा है। लगभग 6.9% हीलियम परमाणु हैं - आवर्त सारणी का दूसरा तत्व।
शेष 0.1% का योगदान अन्य सभी तत्वों से होता है।
पृथ्वी की पपड़ी में रासायनिक तत्वों की प्रचुरता ब्रह्मांड में उनकी प्रचुरता से काफी भिन्न है। पृथ्वी की पपड़ी में सबसे अधिक ऑक्सीजन और सिलिकॉन परमाणु मौजूद हैं। एल्यूमीनियम और लोहे के साथ मिलकर, वे पृथ्वी की पपड़ी के मुख्य यौगिक बनाते हैं। और लोहा और निकल- मुख्य तत्व जो हमारे ग्रह का मूल बनाते हैं।
जीवित जीव भी विभिन्न रासायनिक तत्वों के परमाणुओं से बने होते हैं।मानव शरीर में सबसे अधिक कार्बन, हाइड्रोजन, ऑक्सीजन और नाइट्रोजन परमाणु होते हैं।
रासायनिक तत्वों के बारे में लेख का परिणाम.
- रासायनिक तत्व- एक निश्चित प्रकार का परमाणु
- आज तक, एक व्यक्ति 118 प्रकार के परमाणुओं, यानी 118 रासायनिक तत्वों के अस्तित्व के बारे में विश्वसनीय रूप से जानता है। इनमें से 90 प्रकार के परमाणु प्रकृति में पाए जाते हैं, बाकी कृत्रिम रूप से प्रयोगशालाओं में प्राप्त किए जाते हैं।
- डी.आई. द्वारा रासायनिक तत्वों की आवर्त सारणी के दो संस्करण हैं। मेंडेलीव - अल्पकालिक और दीर्घकालिक
- आधुनिक रासायनिक प्रतीकवाद रासायनिक तत्वों के लैटिन नामों से बना है
- काल- आवर्त सारणी की क्षैतिज रेखाएँ। काल को छोटे और बड़े में विभाजित किया गया है
- समूह- आवर्त सारणी की ऊर्ध्वाधर पंक्तियाँ। समूहों को मुख्य और माध्यमिक में विभाजित किया गया है
द स्केप्टिक केमिस्ट (1661) में। बॉयल ने बताया कि न तो अरस्तू के चार तत्वों और न ही कीमियागरों के तीन सिद्धांतों को तत्व के रूप में पहचाना जा सकता है। बॉयल के अनुसार, तत्व व्यावहारिक रूप से अविभाज्य निकाय (पदार्थ) हैं, जो समान सजातीय (प्राथमिक पदार्थ से युक्त) कणिकाओं से बने होते हैं, जिनसे सभी जटिल निकाय बने होते हैं और जिनमें उन्हें विघटित किया जा सकता है। कणिकाएं आकार, आकार, वजन में भिन्न हो सकती हैं। जिन कणिकाओं से पिंडों का निर्माण होता है वे बाद के परिवर्तनों के दौरान अपरिवर्तित रहते हैं।
हालाँकि, रासायनिक गुणों की आवधिकता को बनाए रखने के लिए, और अनदेखे तत्वों के अनुरूप खाली कोशिकाओं को पेश करने के लिए, मेंडेलीव को परमाणु भार बढ़ाकर वितरित तत्वों के अनुक्रम में कई क्रमपरिवर्तन करने के लिए मजबूर किया गया था। बाद में (20वीं सदी के पहले दशकों में) यह स्पष्ट हो गया कि रासायनिक गुणों की आवधिकता परमाणु क्रमांक (परमाणु नाभिक के आवेश) पर निर्भर करती है, न कि तत्व के परमाणु द्रव्यमान पर। उत्तरार्द्ध तत्व के स्थिर आइसोटोप की संख्या और उनकी प्राकृतिक प्रचुरता से निर्धारित होता है। हालाँकि, किसी तत्व के स्थिर समस्थानिकों का परमाणु द्रव्यमान एक निश्चित मान के आसपास समूहित होता है, क्योंकि नाभिक में न्यूट्रॉन की अधिकता या कमी वाले समस्थानिक अस्थिर होते हैं, और प्रोटॉन की संख्या (अर्थात, परमाणु संख्या) में वृद्धि के साथ, एक स्थिर नाभिक बनाने वाले न्यूट्रॉन की संख्या भी बढ़ जाती है। इसलिए, आवधिक कानून को परमाणु द्रव्यमान पर रासायनिक गुणों की निर्भरता के रूप में भी तैयार किया जा सकता है, हालांकि कई मामलों में इस निर्भरता का उल्लंघन किया जाता है।
आवर्त सारणी में तत्व संख्या के बराबर समान सकारात्मक परमाणु चार्ज की विशेषता वाले परमाणुओं के संग्रह के रूप में एक रासायनिक तत्व की आधुनिक समझ, हेनरी मोसले (1915) और जेम्स चैडविक (1920) के मौलिक कार्य के कारण सामने आई।
ज्ञात रासायनिक तत्व[ | ]
यूरेनियम (ट्रांस्यूरेनियम तत्व) से अधिक परमाणु क्रमांक वाले नए (प्रकृति में नहीं पाए जाने वाले) तत्वों का संश्लेषण शुरू में परमाणु रिएक्टरों में तीव्र न्यूट्रॉन प्रवाह की स्थितियों के तहत और इससे भी अधिक तीव्र - परमाणु (थर्मोन्यूक्लियर) विस्फोट की स्थितियों के तहत यूरेनियम नाभिक द्वारा कई न्यूट्रॉन कैप्चर का उपयोग करके किया गया था। न्यूट्रॉन-समृद्ध नाभिक के बीटा क्षय की बाद की श्रृंखला से परमाणु संख्या में वृद्धि होती है और परमाणु संख्या के साथ बेटी नाभिक की उपस्थिति होती है जेड>92 . इस प्रकार नेपच्यूनियम की खोज की गई ( जेड= 93), प्लूटोनियम (94), अमेरिकियम (95), बर्केलियम (97), आइंस्टीनियम (99) और फ़ेर्मियम (100)। क्यूरियम (96) और कैलिफ़ोर्नियम (98) को भी इस तरह से संश्लेषित (और व्यावहारिक रूप से प्राप्त) किया जा सकता है, लेकिन मूल रूप से उन्हें त्वरक में अल्फा कणों के साथ प्लूटोनियम और क्यूरियम को विकिरणित करके खोजा गया था। मेंडेलीवियम (101) से शुरू होने वाले भारी तत्व, प्रकाश आयनों के साथ एक्टिनाइड लक्ष्यों को विकिरणित करके, केवल त्वरक पर प्राप्त होते हैं।
किसी नए रासायनिक तत्व के लिए नाम प्रस्तावित करने का अधिकार खोजकर्ताओं को दिया जाता है। हालाँकि, इस नाम को कुछ नियमों को पूरा करना होगा। किसी नई खोज की रिपोर्ट की स्वतंत्र प्रयोगशालाओं द्वारा कई वर्षों तक जाँच की जाती है, और, यदि पुष्टि की जाती है, तो इंटरनेशनल यूनियन ऑफ़ प्योर एंड एप्लाइड केमिस्ट्री (IUPAC; इंजी.) द्वारा जाँच की जाती है। इंटरनेशनल यूनियन फॉर प्योर एंड एप्लाइड केमिस्ट्री, IUPAC) आधिकारिक तौर पर नए तत्व के नाम को मंजूरी देता है।
दिसंबर 2016 तक ज्ञात सभी 118 तत्वों के स्थायी नाम IUPAC द्वारा अनुमोदित हैं। खोज आवेदन के क्षण से लेकर IUPAC नाम के अनुमोदन तक, तत्व एक अस्थायी व्यवस्थित नाम के तहत प्रकट होता है, जो लैटिन अंकों से लिया गया है जो तत्व के परमाणु क्रमांक में अंक बनाते हैं, और इन अंकों के पहले अक्षरों से बने तीन-अक्षर वाले अस्थायी प्रतीक द्वारा इंगित किया जाता है। उदाहरण के लिए, 118वें तत्व, ओगेनेसन का, स्थायी नाम की आधिकारिक मंजूरी से पहले, अस्थायी नाम यूनुनोक्टियम और प्रतीक उउओ था।
अनदेखे या अस्वीकृत तत्वों को अक्सर मेंडेलीव द्वारा उपयोग की जाने वाली प्रणाली का उपयोग करके नामित किया जाता है - आवर्त सारणी में बेहतर होमोलॉग के नाम से, उपसर्ग "ईका-" या (शायद ही कभी) "डीवीआई-" के अतिरिक्त, जिसका अर्थ है संस्कृत अंक "एक" और "दो" (यह इस पर निर्भर करता है कि होमोलॉग 1 या 2 अवधि अधिक है)। उदाहरण के लिए, खोज से पहले, जर्मेनियम (सिलिकॉन के नीचे आवर्त सारणी में खड़ा और मेंडेलीव द्वारा भविष्यवाणी की गई) को ईका-सिलिकॉन कहा जाता था, ओगेनेसन (यूनुनोक्टियम, 118) को ईका-रेडॉन भी कहा जाता है, और फ्लेरोवियम (अननक्वाडियम, 114) - ईका-लेड।
वर्गीकरण [ | ]
रासायनिक तत्वों के प्रतीक[ | ]
रासायनिक तत्वों के प्रतीकों का उपयोग तत्वों के नाम के संक्षिप्त रूप में किया जाता है। एक प्रतीक के रूप में, आमतौर पर तत्व के नाम का प्रारंभिक अक्षर लिया जाता है और, यदि आवश्यक हो, तो अगला या निम्नलिखित में से एक जोड़ा जाता है। आमतौर पर ये तत्वों के लैटिन नामों के प्रारंभिक अक्षर हैं: Cu - तांबा ( तांबा), एजी - चांदी ( चांदी), Fe - लौह ( फेरम), औ - सोना ( ऑरम), एचजी - ( हाइड्रार्गिरम). रासायनिक प्रतीकों की ऐसी प्रणाली 1814 में स्वीडिश रसायनज्ञ जे. बर्ज़ेलियस द्वारा प्रस्तावित की गई थी। तत्वों के अस्थायी प्रतीक, उनके स्थायी नामों और प्रतीकों की आधिकारिक मंजूरी से पहले उपयोग किए जाते हैं, जिसमें तीन अक्षर होते हैं, जिसका अर्थ उनके परमाणु संख्या के दशमलव अंकन में तीन अंकों के लैटिन नाम होते हैं (उदाहरण के लिए, यूनुनोक्टियम - 118 वां तत्व - अस्थायी पदनाम यूयूओ था)। ऊपर वर्णित उच्च समरूपों (ईका-आरएन, ईका-पीबी, आदि) के लिए अंकन प्रणाली का भी उपयोग किया जाता है।
तत्व के प्रतीक के पास छोटी संख्याएँ दर्शाई गई हैं: ऊपर बाएँ - परमाणु द्रव्यमान, नीचे बाएँ - क्रम संख्या, ऊपर दाएँ - आयन आवेश, नीचे दाएँ - एक अणु में परमाणुओं की संख्या:
डी. आई. मेंडेलीव की आवधिक प्रणाली में प्लूटोनियम पु (क्रमांक 94) के बाद आने वाले सभी तत्व पृथ्वी की पपड़ी में पूरी तरह से अनुपस्थित हैं, हालांकि उनमें से कुछ सुपरनोवा विस्फोटों के दौरान अंतरिक्ष में बन सकते हैं [ ] . इन तत्वों के सभी ज्ञात समस्थानिकों का अर्ध-जीवन पृथ्वी के जीवनकाल की तुलना में छोटा है। काल्पनिक प्राकृतिक अतिभारी तत्वों की दीर्घकालिक खोजों से अभी तक कोई परिणाम नहीं मिला है।
कुछ सबसे हल्के तत्वों को छोड़कर, अधिकांश रासायनिक तत्व ब्रह्मांड में मुख्य रूप से तारकीय न्यूक्लियोसिंथेसिस के दौरान उत्पन्न हुए (लोहे तक के तत्व - थर्मोन्यूक्लियर संलयन के परिणामस्वरूप, भारी तत्व - परमाणु नाभिक द्वारा न्यूट्रॉन के क्रमिक कब्जे और बाद में बीटा क्षय के साथ-साथ कई अन्य परमाणु प्रतिक्रियाओं में)। सबसे हल्के तत्व (हाइड्रोजन और हीलियम - लगभग पूरी तरह से, लिथियम, बेरिलियम और बोरान - आंशिक रूप से) बिग बैंग (प्राथमिक न्यूक्लियोसिंथेसिस) के बाद पहले तीन मिनट में बने थे।
ब्रह्मांड में विशेष रूप से भारी तत्वों के मुख्य स्रोतों में से एक, गणना के अनुसार, इन तत्वों की महत्वपूर्ण मात्रा की रिहाई के साथ न्यूट्रॉन स्टार विलय होना चाहिए, जो बाद में नए सितारों और उनके ग्रहों के निर्माण में भाग लेते हैं।
रसायनों के अभिन्न अंग के रूप में रासायनिक तत्व[ | ]
रासायनिक तत्व लगभग 500 सरल पदार्थ बनाते हैं। एक तत्व की गुणों में भिन्न विभिन्न सरल पदार्थों के रूप में मौजूद रहने की क्षमता को एलोट्रॉपी कहा जाता है। ज्यादातर मामलों में, साधारण पदार्थों के नाम संबंधित तत्वों (उदाहरण के लिए, जस्ता, एल्यूमीनियम, क्लोरीन) के नाम से मेल खाते हैं, हालांकि, कई एलोट्रोपिक संशोधनों के अस्तित्व के मामले में, एक साधारण पदार्थ और तत्व के नाम भिन्न हो सकते हैं, उदाहरण के लिए, ऑक्सीजन (डाइऑक्सीजन, ओ 2) और ओजोन (ओ 3); हीरा, ग्रेफाइट और कार्बन के कई अन्य एलोट्रोपिक संशोधन कार्बन के अनाकार रूपों के साथ मौजूद हैं।
सामान्य परिस्थितियों में, 11 तत्व गैसीय सरल पदार्थ ( , , , , , , , , , , ) के रूप में मौजूद होते हैं, 2 - तरल पदार्थ ( और ) होते हैं, शेष तत्व ठोस बनाते हैं।
यह सभी देखें [ | ]
रासायनिक तत्व:
लिंक [ | ]
- केद्रोव बी.एम.रसायन विज्ञान में एक तत्व की अवधारणा का विकास। मॉस्को, 1956
- रसायन विज्ञान और जीवन (साल्टर रसायन विज्ञान)। भाग ---- पहला। रसायन शास्त्र की अवधारणाएँ. एम.: आरसीटीयू आईएम का प्रकाशन गृह। डी. आई. मेंडेलीव, 1997
- अजीमोव ए.रसायन शास्त्र का संक्षिप्त इतिहास. सेंट पीटर्सबर्ग, एम्फोरा, 2002
- बेदन्याकोव वी. ए. "रासायनिक तत्वों की उत्पत्ति पर" ई. च. ए. हां., खंड 33 (2002), भाग 4 पृ. 914-963।
टिप्पणियाँ [ | ]
- लेखकों की टीम. महान सोवियत विश्वकोश में "रासायनिक तत्व" शब्द का अर्थ (अनिश्चित) . सोवियत विश्वकोश. 16 मई 2014 को मूल से संग्रहीत।
- परमाणु और रासायनिक तत्व.
- अकार्बनिक पदार्थों के वर्ग.
- , साथ। 266-267.
- परमाणु संख्या 113, 115, 117 और 118 वाले तत्वों की खोज और निर्धारण (अनिश्चित) .
- दुनिया भर में - रासायनिक तत्व
- रसायन विज्ञान की बुनियादी अवधारणाएँ।
- मारिनोव, ए.; रोडुस्किन, आई.; कोल्ब, डी.; पपी, ए.; काशिव, वाई.; ब्रांट, आर.; जेंट्री, आर.वी.; मिलर, एच.डब्ल्यू.प्राकृतिक Th (अंग्रेजी) // ArXiv.org: जर्नल में परमाणु द्रव्यमान संख्या A=292 और परमाणु संख्या Z=~122 के साथ लंबे समय तक जीवित रहने वाले अतिभारी नाभिक के लिए साक्ष्य। - 2008.
- कॉस्मिक किरणों में पाए जाने वाले अतिभारी तत्व //lenta.ru। - 2011.
- प्राइमर्डियल प्लूटोनियम-244 के अंशों को छोड़कर, जिसका आधा जीवन 80 मिलियन वर्ष है; प्लूटोनियम#प्राकृतिक प्लूटोनियम देखें।
- हॉफमैन, डी.सी.; लॉरेंस, एफ.ओ.; मेव्हर्टर, जे.एल.; राउरके, एफ.एम.प्रकृति में प्लूटोनियम-244 का पता लगाना // प्रकृति: लेख। - 1971. - इस्स। 234 . - पी. 132-134. - डीओआई:10.1038/234132ए0।
- रीटा कॉर्नेलिस, जो कारुसो, हेलेन क्रूज़, क्लॉस ह्यूमैन।मौलिक विशिष्टता II की पुस्तिका: पर्यावरण, भोजन, चिकित्सा और व्यावसायिक स्वास्थ्य में प्रजातियां। - जॉन विले एंड संस, 2005. - 768 पी। - आईएसबीएन 0470855983, 9780470855980।
- हबल ने पहला किलोनोवा खोजा, 8 अगस्त 2013 को संग्रहीत। // compulenta.computerra.ru
- 30 जनवरी 2009 वेबैक मशीन पर (21-05-2013 से अनुपलब्ध लिंक - , ).
साहित्य [ | ]
- मेंडेलीव डी.आई.,.// ब्रोकहॉस और एफ्रॉन का विश्वकोश शब्दकोश: 86 खंडों में (82 खंड और 4 अतिरिक्त)। - सेंट पीटर्सबर्ग। , 1890-1907.
- चेर्नोबेल्स्काया जी.एम.हाई स्कूल में रसायन विज्ञान पढ़ाने की विधियाँ। - एम.: मानवतावादी प्रकाशन केंद्र VLADOS, 2000. - 336 पी। - आईएसबीएन 5-691-00492-1।
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
हमारे चारों ओर प्रकृति की सारी विविधता अपेक्षाकृत कम संख्या में रासायनिक तत्वों के संयोजन से बनी है। तो एक रासायनिक तत्व की विशेषता क्या है, और यह एक साधारण पदार्थ से कैसे भिन्न है?
रासायनिक तत्व: खोज का इतिहास
विभिन्न ऐतिहासिक युगों में, "तत्व" की अवधारणा में अलग-अलग अर्थ रखे गए थे। प्राचीन यूनानी दार्शनिक 4 "तत्वों" को ऐसे "तत्व" मानते थे - गर्मी, सर्दी, सूखापन और नमी। जोड़े में मिलकर, उन्होंने दुनिया में हर चीज़ की चार "शुरुआत" बनाई - अग्नि, वायु, जल और पृथ्वी।
17वीं शताब्दी में आर. बॉयल ने बताया कि सभी तत्व भौतिक प्रकृति के हैं और उनकी संख्या काफी बड़ी हो सकती है।
1787 में, फ्रांसीसी रसायनज्ञ ए. लावोइसियर ने "सरल निकायों की तालिका" बनाई। इसमें उस समय तक ज्ञात सभी तत्व शामिल थे। उत्तरार्द्ध को सरल निकायों के रूप में समझा जाता था जिन्हें रासायनिक तरीकों से और भी सरल तरीकों से विघटित नहीं किया जा सकता था। इसके बाद, यह पता चला कि तालिका में कुछ जटिल पदार्थ शामिल थे।
जब डी. आई. मेंडेलीव ने आवर्त नियम की खोज की, तब तक केवल 63 रासायनिक तत्व ज्ञात थे। वैज्ञानिक की खोज से न केवल रासायनिक तत्वों का एक व्यवस्थित वर्गीकरण हुआ, बल्कि नए, अभी तक खोजे नहीं गए तत्वों के अस्तित्व की भविष्यवाणी करने में भी मदद मिली।

चावल। 1. ए. लवॉज़िएर।
रासायनिक तत्व क्या है?
एक निश्चित प्रकार के परमाणु को रासायनिक तत्व कहा जाता है। वर्तमान में, 118 रासायनिक तत्व ज्ञात हैं। प्रत्येक तत्व को एक प्रतीक द्वारा दर्शाया जाता है जो उसके लैटिन नाम से एक या दो अक्षरों का प्रतिनिधित्व करता है। उदाहरण के लिए, तत्व हाइड्रोजन को लैटिन अक्षर H और सूत्र H 2 द्वारा निरूपित किया जाता है - तत्व हाइड्रोजेनियम के लैटिन नाम का पहला अक्षर। सभी पर्याप्त रूप से अच्छी तरह से अध्ययन किए गए तत्वों के प्रतीक और नाम हैं जो आवर्त सारणी के मुख्य और माध्यमिक उपसमूहों में पाए जा सकते हैं, जहां वे सभी एक निश्चित क्रम में व्यवस्थित हैं।
💡
प्रणालियाँ कई प्रकार की होती हैं, लेकिन आम तौर पर स्वीकृत डी. आई. मेंडेलीव की रासायनिक तत्वों की आवर्त प्रणाली है, जो डी. आई. मेंडेलीव के आवर्त नियम की एक ग्राफिकल अभिव्यक्ति है। आमतौर पर आवर्त सारणी के छोटे और लंबे रूपों का उपयोग किया जाता है।

चावल। 2. डी. आई. मेंडेलीव के तत्वों की आवधिक प्रणाली।
वह मुख्य विशेषता क्या है जिसके द्वारा एक परमाणु को किसी विशेष तत्व के लिए जिम्मेदार ठहराया जाता है? डी. आई. मेंडेलीव और 19वीं शताब्दी के अन्य रसायनज्ञों ने परमाणु की मुख्य विशेषता द्रव्यमान को इसकी सबसे स्थिर विशेषता माना, इसलिए आवर्त सारणी में तत्वों को परमाणु द्रव्यमान के आरोही क्रम में व्यवस्थित किया गया है (कुछ अपवादों के साथ)।
आधुनिक अवधारणाओं के अनुसार, किसी परमाणु का मुख्य गुण, उसे किसी विशेष तत्व से संबंधित करना, नाभिक का आवेश है। इस प्रकार, एक रासायनिक तत्व एक प्रकार का परमाणु है जो रासायनिक तत्व के भाग के एक निश्चित मूल्य (मूल्य) द्वारा विशेषता है - नाभिक का सकारात्मक चार्ज।
सभी मौजूदा 118 रासायनिक तत्वों में से अधिकांश (लगभग 90) प्रकृति में पाए जा सकते हैं। बाकी परमाणु प्रतिक्रियाओं का उपयोग करके कृत्रिम रूप से प्राप्त किए जाते हैं। तत्व 104-107 को डुबना में संयुक्त परमाणु अनुसंधान संस्थान में भौतिकविदों द्वारा संश्लेषित किया गया था। वर्तमान में, उच्च क्रम संख्या वाले रासायनिक तत्वों के कृत्रिम उत्पादन पर काम जारी है।
सभी तत्वों को धातु और अधातु में विभाजित किया गया है। 80 से अधिक तत्व धातु हैं। हालाँकि, यह विभाजन सशर्त है। कुछ शर्तों के तहत, कुछ धातुएँ गैर-धातु गुण प्रदर्शित कर सकती हैं, और कुछ गैर-धातुएँ धात्विक गुण प्रदर्शित कर सकती हैं।
प्राकृतिक वस्तुओं में विभिन्न तत्वों की सामग्री व्यापक रूप से भिन्न होती है। 8 रासायनिक तत्व (ऑक्सीजन, सिलिकॉन, एल्यूमीनियम, लोहा, कैल्शियम, सोडियम, पोटेशियम, मैग्नीशियम) द्रव्यमान के हिसाब से पृथ्वी की पपड़ी का 99% हिस्सा बनाते हैं, बाकी सभी 1% से कम हैं। अधिकांश रासायनिक तत्व प्राकृतिक उत्पत्ति (95) के हैं, हालांकि उनमें से कुछ मूल रूप से कृत्रिम रूप से प्राप्त किए गए थे (उदाहरण के लिए, प्रोमेथियम)।
"सरल पदार्थ" और "रासायनिक तत्व" की अवधारणाओं के बीच अंतर करना आवश्यक है। एक साधारण पदार्थ की विशेषता कुछ रासायनिक और भौतिक गुण होते हैं। रासायनिक परिवर्तन की प्रक्रिया में एक साधारण पदार्थ अपने कुछ गुण खो देता है और तत्व के रूप में एक नये पदार्थ में प्रवेश कर जाता है। उदाहरण के लिए, नाइट्रोजन और हाइड्रोजन, जो अमोनिया का हिस्सा हैं, इसमें साधारण पदार्थों के रूप में नहीं, बल्कि तत्वों के रूप में निहित हैं।
कुछ तत्वों को समूहों में संयोजित किया जाता है, जैसे ऑर्गेनोजेन (कार्बन, ऑक्सीजन, हाइड्रोजन, नाइट्रोजन), क्षार धातु (लिथियम, सोडियम, पोटेशियम, आदि), लैंथेनाइड्स (लैंथेनम, सेरियम, आदि), हैलोजन (फ्लोरीन, क्लोरीन, ब्रोमीन, आदि), अक्रिय तत्व (हीलियम, नियॉन, आर्गन)

चावल। 3. हैलोजन तालिका.
हमने क्या सीखा?
8वीं कक्षा का रसायन विज्ञान पाठ्यक्रम शुरू करते समय, सबसे पहले "रासायनिक तत्व" की अवधारणा का अध्ययन करना आवश्यक है। वर्तमान में, 118 रासायनिक तत्व ज्ञात हैं, जिन्हें परमाणु द्रव्यमान में वृद्धि के अनुसार डी. आई. मेंडेलीव की तालिका में व्यवस्थित किया गया है, और जिनमें मूल अम्लीय गुण हैं।
विषय प्रश्नोत्तरी
रिपोर्ट मूल्यांकन
औसत श्रेणी: 4.2. कुल प्राप्त रेटिंग: 371.
रासायनिक तत्व एक सामूहिक शब्द है जो एक साधारण पदार्थ के परमाणुओं के एक समूह का वर्णन करता है, अर्थात, जिसे किसी भी सरल (उनके अणुओं की संरचना के अनुसार) घटकों में विभाजित नहीं किया जा सकता है। कल्पना करें कि आपको रसायनज्ञों द्वारा आविष्कृत किसी उपकरण या विधि का उपयोग करके इसे काल्पनिक घटकों में विभाजित करने के अनुरोध के साथ शुद्ध लोहे का एक टुकड़ा प्राप्त होता है। हालाँकि, आप कुछ नहीं कर सकते, लोहे को कभी भी किसी सरल चीज़ में विभाजित नहीं किया जाएगा। एक साधारण पदार्थ - लोहा - रासायनिक तत्व Fe से मेल खाता है।
सैद्धांतिक परिभाषा
ऊपर बताए गए प्रायोगिक तथ्य को निम्नलिखित परिभाषा का उपयोग करके समझाया जा सकता है: एक रासायनिक तत्व संबंधित सरल पदार्थ के परमाणुओं (अणुओं नहीं!) का एक अमूर्त संग्रह है, यानी एक ही प्रकार के परमाणु। यदि ऊपर वर्णित शुद्ध लोहे के टुकड़े में प्रत्येक व्यक्तिगत परमाणु को देखने का कोई तरीका होता, तो वे सभी एक ही होते - लोहे के परमाणु। इसके विपरीत, एक रासायनिक यौगिक, जैसे कि आयरन ऑक्साइड, में हमेशा कम से कम दो अलग-अलग प्रकार के परमाणु होते हैं: लौह परमाणु और ऑक्सीजन परमाणु।
शर्तें जो आपको पता होनी चाहिए
परमाणु भार: प्रोटॉन, न्यूट्रॉन और इलेक्ट्रॉनों का द्रव्यमान जो एक रासायनिक तत्व का परमाणु बनाते हैं।
परमाणु संख्या: किसी तत्व के परमाणु के नाभिक में प्रोटॉनों की संख्या।
रासायनिक प्रतीक: दिए गए तत्व के पदनाम का प्रतिनिधित्व करने वाला एक अक्षर या लैटिन अक्षरों का जोड़ा।
रासायनिक यौगिक: वह पदार्थ जिसमें दो या दो से अधिक रासायनिक तत्व एक निश्चित अनुपात में एक दूसरे से जुड़े होते हैं।
धातु: एक तत्व जो अन्य तत्वों के साथ रासायनिक प्रतिक्रियाओं में इलेक्ट्रॉन खो देता है।
धातु के रूप-रंग का एक अधातु पदार्थ: एक तत्व जो कभी धातु और कभी अधातु के रूप में प्रतिक्रिया करता है।
नांमेटल: एक तत्व जो अन्य तत्वों के साथ रासायनिक प्रतिक्रियाओं में इलेक्ट्रॉन प्राप्त करना चाहता है।
रासायनिक तत्वों की आवधिक प्रणाली: रासायनिक तत्वों को उनके परमाणु क्रमांक के अनुसार वर्गीकृत करने की एक प्रणाली।
कृत्रिम तत्व: वह जो प्रयोगशाला में कृत्रिम रूप से प्राप्त किया जाता है, और आमतौर पर प्रकृति में नहीं होता है।

प्राकृतिक और कृत्रिम तत्व
92 रासायनिक तत्व पृथ्वी पर प्राकृतिक रूप से पाए जाते हैं। बाकी प्रयोगशालाओं में कृत्रिम रूप से प्राप्त किए गए थे। एक सिंथेटिक रासायनिक तत्व आम तौर पर कण त्वरक (इलेक्ट्रॉन और प्रोटॉन जैसे उप-परमाणु कणों की गति बढ़ाने के लिए उपयोग किए जाने वाले उपकरण) या परमाणु रिएक्टर (परमाणु प्रतिक्रियाओं में जारी ऊर्जा को नियंत्रित करने के लिए उपयोग किए जाने वाले उपकरण) में परमाणु प्रतिक्रियाओं का उत्पाद होता है। परमाणु संख्या 43 के साथ प्राप्त पहला सिंथेटिक तत्व टेक्नेटियम था, जिसे 1937 में इतालवी भौतिकविदों सी. पेरियर और ई. सेग्रे द्वारा खोजा गया था। टेक्नेटियम और प्रोमेथियम के अलावा, सभी सिंथेटिक तत्वों के नाभिक यूरेनियम से बड़े होते हैं। अंतिम सिंथेटिक तत्व का नाम लिवरमोरियम (116) है, और उससे पहले फ्लेरोवियम (114) था।

दो दर्जन सामान्य एवं महत्वपूर्ण तत्व
| नाम | प्रतीक | सभी परमाणुओं का प्रतिशत * | रासायनिक तत्वों के गुण (सामान्य कमरे की स्थिति में) |
|||
| ब्रह्मांड में | पृथ्वी की पपड़ी में | समुद्र के पानी में | मानव शरीर में |
|||
| अल्युमीनियम | अल | - | 6,3 | - | - | हल्का, चांदी धातु |
| कैल्शियम | सीए | - | 2,1 | - | 0,02 | प्राकृतिक खनिज, सीपियाँ, हड्डियाँ शामिल हैं |
| कार्बन | साथ | - | - | - | 10,7 | सभी जीवित प्राणियों का आधार |
| क्लोरीन | क्लोरीन | - | - | 0,3 | - | जहरीली गैस |
| ताँबा | घन | - | - | - | - | केवल लाल धातु |
| सोना | ए.यू. | - | - | - | - | केवल पीली धातु |
| हीलियम | वह | 7,1 | - | - | - | बहुत हल्की गैस |
| हाइड्रोजन | एच | 92,8 | 2,9 | 66,2 | 60,6 | सभी तत्वों में सबसे हल्का; गैस |
| आयोडीन | मैं | - | - | - | - | अधातु; एक एंटीसेप्टिक के रूप में उपयोग किया जाता है |
| लोहा | फ़े | - | 2,1 | - | - | चुंबकीय धातु; लोहा और इस्पात के उत्पादन के लिए उपयोग किया जाता है |
| नेतृत्व करना | पंजाब | - | - | - | - | नरम, भारी धातु |
| मैगनीशियम | एमजी | - | 2,0 | - | - | बहुत हल्की धातु |
| बुध | एचजी | - | - | - | - | तरल धातु; दो तरल तत्वों में से एक |
| निकल | नी | - | - | - | - | संक्षारण प्रतिरोधी धातु; सिक्कों में प्रयोग किया जाता है |
| नाइट्रोजन | एन | - | - | - | 2,4 | गैस, वायु का मुख्य घटक |
| ऑक्सीजन | के बारे में | - | 60,1 | 33,1 | 25,7 | गैस, दूसरा महत्वपूर्ण वायु घटक |
| फास्फोरस | आर | - | - | - | 0,1 | अधातु; पौधों के लिए महत्वपूर्ण |
| पोटैशियम | को | - | 1.1 | - | - | धातु; पौधों के लिए महत्वपूर्ण; आमतौर पर इसे "पोटाश" कहा जाता है |
* यदि मान निर्दिष्ट नहीं है, तो तत्व 0.1 प्रतिशत से कम है।
पदार्थ के निर्माण का मूल कारण बिग बैंग है
ब्रह्मांड में सबसे पहले कौन सा रासायनिक तत्व था? वैज्ञानिकों का मानना है कि इस प्रश्न का उत्तर तारों और उन प्रक्रियाओं में निहित है जिनसे तारे बनते हैं। ऐसा माना जाता है कि ब्रह्माण्ड की उत्पत्ति 12 से 15 अरब वर्ष पूर्व किसी समय हुई थी। इस क्षण तक, ऊर्जा के अलावा किसी भी चीज़ की कल्पना नहीं की गई है। लेकिन कुछ ऐसा हुआ जिसने इस ऊर्जा को एक विशाल विस्फोट (तथाकथित बिग बैंग) में बदल दिया। बिग बैंग के बाद के कुछ ही सेकंड में पदार्थ बनना शुरू हो गया।
पदार्थ के प्रकट होने वाले पहले सरलतम रूप प्रोटॉन और इलेक्ट्रॉन थे। उनमें से कुछ हाइड्रोजन परमाणुओं में संयुक्त होते हैं। उत्तरार्द्ध में एक प्रोटॉन और एक इलेक्ट्रॉन होता है; यह सबसे सरल परमाणु है जिसका अस्तित्व हो सकता है।

धीरे-धीरे, लंबे समय में, हाइड्रोजन परमाणु अंतरिक्ष के कुछ क्षेत्रों में एक साथ इकट्ठा होने लगे, जिससे घने बादल बन गए। इन बादलों में हाइड्रोजन को गुरुत्वाकर्षण बलों द्वारा कॉम्पैक्ट संरचनाओं में खींच लिया गया था। अंततः हाइड्रोजन के ये बादल इतने घने हो गए कि तारे बन गए।
नये तत्वों के रासायनिक रिएक्टर के रूप में तारे
तारा केवल पदार्थ का एक द्रव्यमान है जो परमाणु प्रतिक्रियाओं की ऊर्जा उत्पन्न करता है। इन प्रतिक्रियाओं में सबसे आम है एक हीलियम परमाणु बनाने के लिए चार हाइड्रोजन परमाणुओं का संयोजन। जैसे ही तारे बनने शुरू हुए, हीलियम ब्रह्मांड में प्रकट होने वाला दूसरा तत्व बन गया।
जैसे-जैसे तारे पुराने होते जाते हैं, वे हाइड्रोजन-हीलियम परमाणु प्रतिक्रियाओं से अन्य प्रकार की प्रतिक्रियाओं में बदल जाते हैं। इनमें हीलियम परमाणु कार्बन परमाणु बनाते हैं। बाद में कार्बन परमाणु ऑक्सीजन, नियॉन, सोडियम और मैग्नीशियम बनाते हैं। फिर भी बाद में, नियॉन और ऑक्सीजन एक दूसरे के साथ मिलकर मैग्नीशियम बनाते हैं। जैसे-जैसे ये प्रतिक्रियाएँ जारी रहती हैं, अधिक से अधिक रासायनिक तत्व बनते हैं।
रासायनिक तत्वों की पहली प्रणाली
200 साल पहले, रसायनज्ञों ने उन्हें वर्गीकृत करने के तरीकों की तलाश शुरू कर दी थी। उन्नीसवीं सदी के मध्य में लगभग 50 रासायनिक तत्व ज्ञात थे। उन प्रश्नों में से एक जिसे रसायनशास्त्री हल करना चाहते थे। निम्नलिखित तक उबाला गया: क्या एक रासायनिक तत्व किसी अन्य तत्व से पूरी तरह से अलग पदार्थ है? या क्या कुछ तत्व किसी तरह से दूसरों से संबंधित हैं? क्या कोई सामान्य कानून है जो उन्हें एकजुट करता है?
रसायनज्ञों ने रासायनिक तत्वों की विभिन्न प्रणालियाँ प्रस्तावित की हैं। इसलिए, उदाहरण के लिए, 1815 में अंग्रेजी रसायनज्ञ विलियम प्राउट ने सुझाव दिया कि सभी तत्वों के परमाणु द्रव्यमान हाइड्रोजन परमाणु के द्रव्यमान के गुणक हैं, यदि हम इसे एक के बराबर लेते हैं, अर्थात, वे पूर्णांक होने चाहिए। उस समय, कई तत्वों के परमाणु द्रव्यमान की गणना हाइड्रोजन के द्रव्यमान के संबंध में जे. डाल्टन द्वारा पहले ही की जा चुकी थी। हालाँकि, यदि यह लगभग कार्बन, नाइट्रोजन, ऑक्सीजन का मामला है, तो 35.5 के द्रव्यमान वाला क्लोरीन इस योजना में फिट नहीं होता है।
जर्मन रसायनज्ञ जोहान वोल्फगैंग डोबेराइनर (1780-1849) ने 1829 में दिखाया कि तथाकथित हैलोजन समूह (क्लोरीन, ब्रोमीन और आयोडीन) के तीन तत्वों को उनके सापेक्ष परमाणु द्रव्यमान के आधार पर वर्गीकृत किया जा सकता है। ब्रोमीन (79.9) का परमाणु भार क्लोरीन (35.5) और आयोडीन (127) के परमाणु भार के लगभग औसत के बराबर निकला, अर्थात् 35.5 + 127 ÷ 2 = 81.25 (79.9 के करीब)। रासायनिक तत्वों के समूहों में से किसी एक के निर्माण के लिए यह पहला दृष्टिकोण था। डोबेरिनर ने ऐसे दो और तत्वों के त्रिक की खोज की, लेकिन वह एक सामान्य आवधिक कानून बनाने में विफल रहे।
रासायनिक तत्वों की आवर्त सारणी कैसे प्रकट हुई?
अधिकांश प्रारंभिक वर्गीकरण योजनाएँ बहुत सफल नहीं थीं। फिर, 1869 के आसपास, लगभग एक ही समय में दो रसायनज्ञों ने एक ही तरह की खोज की। रूसी रसायनज्ञ दिमित्री मेंडेलीव (1834-1907) और जर्मन रसायनज्ञ जूलियस लोथर मेयर (1830-1895) ने समान भौतिक और रासायनिक गुणों वाले तत्वों को समूहों, श्रृंखलाओं और अवधियों की एक क्रमबद्ध प्रणाली में व्यवस्थित करने का प्रस्ताव रखा। साथ ही, मेंडेलीव और मेयर ने बताया कि रासायनिक तत्वों के गुण उनके परमाणु भार के आधार पर समय-समय पर दोहराए जाते हैं।
आज, मेंडेलीव को आम तौर पर आवधिक कानून का खोजकर्ता माना जाता है क्योंकि उन्होंने एक कदम उठाया जो मेयर ने नहीं उठाया। जब सभी तत्व आवर्त सारणी में स्थित हो गये तो उसमें कुछ अंतराल आ गये। मेंडेलीव ने भविष्यवाणी की थी कि ये ऐसे तत्वों के स्थल थे जिनकी अभी तक खोज नहीं हुई थी।
हालाँकि, वह और भी आगे बढ़ गया। मेंडेलीव ने इन अभी तक खोजे नहीं गए तत्वों के गुणों की भविष्यवाणी की थी। वह जानता था कि वे आवर्त सारणी में कहाँ स्थित हैं, इसलिए वह उनके गुणों का अनुमान लगा सकता था। यह उल्लेखनीय है कि मेंडेलीव द्वारा पूर्वानुमानित प्रत्येक रासायनिक तत्व, भविष्य के गैलियम, स्कैंडियम और जर्मेनियम की खोज आवधिक कानून प्रकाशित करने के दस साल से भी कम समय के बाद की गई थी।
आवर्त सारणी का संक्षिप्त रूप
यह गणना करने का प्रयास किया गया कि विभिन्न वैज्ञानिकों द्वारा आवधिक प्रणाली के ग्राफिक प्रतिनिधित्व के कितने प्रकार प्रस्तावित किए गए थे। यह 500 से अधिक निकला। इसके अलावा, विकल्पों की कुल संख्या का 80% टेबल हैं, और बाकी ज्यामितीय आकार, गणितीय वक्र आदि हैं। परिणामस्वरूप, चार प्रकार की टेबलों को व्यावहारिक अनुप्रयोग मिला है: छोटी, अर्ध-लंबी, लंबी और सीढ़ी (पिरामिड)। उत्तरार्द्ध का प्रस्ताव महान भौतिक विज्ञानी एन. बोह्र द्वारा किया गया था।
नीचे दिया गया चित्र संक्षिप्त रूप दिखाता है।

इसमें रासायनिक तत्वों को बाएं से दाएं और ऊपर से नीचे तक उनके परमाणु क्रमांक के आरोही क्रम में व्यवस्थित किया जाता है। तो, आवर्त सारणी के पहले रासायनिक तत्व, हाइड्रोजन का परमाणु क्रमांक 1 है क्योंकि हाइड्रोजन परमाणुओं के नाभिक में एक और केवल एक प्रोटॉन होता है। इसी प्रकार, ऑक्सीजन की परमाणु संख्या 8 है, क्योंकि सभी ऑक्सीजन परमाणुओं के नाभिक में 8 प्रोटॉन होते हैं (नीचे चित्र देखें)।

आवर्त प्रणाली के मुख्य संरचनात्मक टुकड़े आवर्त और तत्वों के समूह हैं। छह अवधियों में, सभी कोशिकाएँ भर जाती हैं, सातवीं अभी तक पूरी नहीं हुई है (तत्व 113, 115, 117 और 118, हालांकि प्रयोगशालाओं में संश्लेषित हैं, अभी तक आधिकारिक तौर पर पंजीकृत नहीं हुए हैं और उनके नाम नहीं हैं)।
समूहों को मुख्य (ए) और माध्यमिक (बी) उपसमूहों में विभाजित किया गया है। पहले तीन आवर्तों के तत्व, जिनमें प्रत्येक में एक श्रृंखला-पंक्ति होती है, विशेष रूप से ए-उपसमूहों में शामिल होते हैं। शेष चार अवधियों में प्रत्येक में दो पंक्तियाँ शामिल हैं।
एक ही समूह के रासायनिक तत्वों में समान रासायनिक गुण होते हैं। तो, पहले समूह में क्षार धातुएँ हैं, दूसरे में - क्षारीय पृथ्वी। समान अवधि के तत्वों में ऐसे गुण होते हैं जो धीरे-धीरे क्षार धातु से उत्कृष्ट गैस में बदल जाते हैं। नीचे दिया गया चित्र दिखाता है कि तालिका में अलग-अलग तत्वों के लिए गुणों में से एक - परमाणु त्रिज्या - कैसे बदलता है।
आवर्त सारणी का दीर्घावधि रूप
इसे नीचे दिए गए चित्र में दिखाया गया है और इसे पंक्तियों और स्तंभों द्वारा दो दिशाओं में विभाजित किया गया है। इसमें सात अवधि पंक्तियाँ हैं, जैसा कि संक्षिप्त रूप में है, और 18 स्तंभ हैं, जिन्हें समूह या परिवार कहा जाता है। वास्तव में, समूहों की संख्या में लघु रूप में 8 से लेकर दीर्घ रूप में 18 तक की वृद्धि सभी तत्वों को 4 से शुरू होने वाले आवर्तों में दो में नहीं, बल्कि एक पंक्ति में रखकर प्राप्त की जाती है।
समूहों के लिए दो अलग-अलग नंबरिंग प्रणालियों का उपयोग किया जाता है, जैसा कि तालिका के शीर्ष पर दिखाया गया है। रोमन अंक प्रणाली (आईए, आईआईए, आईआईबी, आईवीबी, आदि) पारंपरिक रूप से अमेरिका में लोकप्रिय रही है। एक अन्य प्रणाली (1, 2, 3, 4, आदि) पारंपरिक रूप से यूरोप में उपयोग की जाती है, और कुछ साल पहले संयुक्त राज्य अमेरिका में उपयोग के लिए अनुशंसित की गई थी।

उपरोक्त आंकड़ों में आवर्त सारणी की उपस्थिति थोड़ी भ्रामक है, जैसा कि ऐसी किसी भी प्रकाशित तालिका के साथ होता है। इसका कारण यह है कि तालिकाओं के नीचे दिखाए गए तत्वों के दो समूह वास्तव में उनके भीतर स्थित होने चाहिए। उदाहरण के लिए, लैंथेनाइड्स, बेरियम (56) और हेफ़नियम (72) के बीच की अवधि 6 से संबंधित हैं। इसके अलावा, एक्टिनाइड्स रेडियम (88) और रदरफोर्डियम (104) के बीच की अवधि 7 से संबंधित हैं। यदि उन्हें किसी मेज पर चिपका दिया जाए, तो यह कागज के टुकड़े या दीवार चार्ट पर फिट होने के लिए बहुत चौड़ा होगा। इसलिए, इन तत्वों को तालिका के नीचे रखने की प्रथा है।
यह भी देखें: परमाणु संख्या के आधार पर रासायनिक तत्वों की सूची और रासायनिक तत्वों की वर्णमाला सूची सामग्री 1 वर्तमान में उपयोग किए जाने वाले प्रतीक... विकिपीडिया
यह भी देखें: प्रतीक द्वारा रासायनिक तत्वों की सूची और रासायनिक तत्वों की वर्णमाला सूची यह परमाणु संख्या के आरोही क्रम में व्यवस्थित रासायनिक तत्वों की एक सूची है। तालिका ... विकिपीडिया में तत्व, प्रतीक, समूह और अवधि का नाम दिखाती है
- (आईएसओ 4217) मुद्राओं और निधियों के प्रतिनिधित्व के लिए कोड (इंग्लैंड) कोड पोर ला रिप्रजेंटेशन डेस मोनाईज़ एट टाइप्स डी फोंड्स (एफआर) ... विकिपीडिया
पदार्थ का सबसे सरल रूप जिसे रासायनिक विधियों द्वारा पहचाना जा सकता है। ये सरल और जटिल पदार्थों के घटक भाग हैं, जो समान परमाणु आवेश वाले परमाणुओं का संग्रह हैं। किसी परमाणु के नाभिक का आवेश उसमें मौजूद प्रोटॉनों की संख्या से निर्धारित होता है... कोलियर इनसाइक्लोपीडिया
सामग्री 1 पुरापाषाण युग 2 10वीं सहस्राब्दी ईसा पूर्व इ। 3 9वीं सहस्राब्दी ई.पू एर ... विकिपीडिया
सामग्री 1 पुरापाषाण युग 2 10वीं सहस्राब्दी ईसा पूर्व इ। 3 9वीं सहस्राब्दी ई.पू एर ... विकिपीडिया
इस शब्द के अन्य अर्थ हैं, रूसी (अर्थ) देखें। रूसी ... विकिपीडिया
शब्दावली 1: :dw सप्ताह के दिन की संख्या। "1" विभिन्न दस्तावेज़ों से सोमवार शब्द परिभाषाओं से मेल खाता है: डीडब्ल्यू डीयूटी मॉस्को और यूटीसी के बीच अंतर, घंटों की पूर्णांक संख्या के रूप में व्यक्त किया गया शब्द परिभाषाएँ ... ... मानक और तकनीकी दस्तावेज़ीकरण की शर्तों की शब्दकोश-संदर्भ पुस्तक