Конфігурація макромолекул та стереоізомери. Конформація та гнучкість макромолекул
Класифікація полімерів за хімічною будовою основного ланцюга та макромолекули в цілому. Міжмолекулярна взаємодія у полімерах. Поняття густини енергії когезії та параметра розчинності.
Структура макромолекулвключає їх хімічну будову та довжину, розподіл за довжинами та молекулярними масами, форму та просторове розташування ланок. За хімічною будовою основного ланцюга розрізняють гомоцепні (з ланцюгом з атомів вуглецю - карбоцепні ) та гетероцепні полімери, а за хімічною будовою макромолекул загалом – полімери:
· органічні - ланцюг складається з атомів вуглецю, кисню, азоту та сірки;
· елементоорганічні - Ланцюг складається з кремнію, фосфору та інших атомів, до яких приєднані вуглецеві атоми або групи, або навпаки;
· неорганічні - повністю відсутні атоми вуглецю або карбоцепні з кратними (подвійними або потрійними) зв'язками без бічних груп.
Найбільш поширені органічні карбоцепні полімери, що включають і різні їх похідні (галогенсодержащіе, ефіри, спирти, кислоти та ін), назва яких утворюється назвою мономеру з приставкою «полі». До граничних аліфатичних карбоцепних полімерів відносяться поліетилен, поліпропілен, полівінілхлорид, політетрафторетилен, політрифторхлоретилен, полівініловий спирт, полівінілацетат, поліакриламід, поліакрилонітрил, поліметилметакрилат та інші. Ненасиченими є полібутадієн, поліізопрен і поліхлоропрен, прикладом жирноароматичних полімерів - поліетиленфенілен, а ароматичних - поліфенілен. Число неорганічних гомоланцюгових полімерів обмежено - карбоцепні карбін (~C≡C-C≡C~) і кумулен (=С=С=С=), а також полісера (~S-S-S~), полісилан (~SiH 2 -SiH 2 ~), полігерман (~GeH 2 -GeH 2 ~) та ін. Більш поширені елементоорганічні гомоцепні полімери з органічних ланцюгів (карболанцюгові) з елементоорганічними бічними групами або з неорганічних ланцюгів з органічними радикалами: полівінілалкілсилани, поліоргансилани, полімери, що містять бор. Органічні гетероцепні полімери поділяють на класи залежно від природи функціональних груп основний ланцюга. Вони можуть бути аліфатичними або ароматичними залежно від будови вуглеводневих груп між функціональними групами (табл.1.1).
Таблиця 1.1.
Гетероцепні полімери різних класів:
| Функціональна група | Полімер | |
| Назва класу | Представники | |
| К і с л о р о д с д е рж а щ е | ||
| Проста ефірна | Прості поліефіри | Поліметиленоксид (~CH 2 -O~) |
| Поліетиленоксид (~CH 2 -CH 2 -O~) | ||
| Складноефірна | Складні поліефіри | Поліетилентерефталат ([-СН 2 -СН 2 -О-ОС-Ar-СО-О-] n) |
| Поліарилати ([-ОС-R-СОО-R`-О-] n) | ||
| Полікарбонати ([-О-Ar-CH 2 -Ar-O-CO-O-Ar-CH 2 -Ar-] n) | ||
| А з т о д о т рж а щ я | ||
| Ацетальна | Ацеталі | Целюлоза (C 6 Н 1 0 Про 5) n |
| Амідна | Поліаміди (-СО-NН-) | Полігексаметиленадипамід |
| Імідна | Полііміди | Поліпіромелітімід |
| Сечовинова | Полимочевина | Полінонаметиленсечовина |
| Уретана | Поліуретани (–HN-CO-O) | ~(CH 2) 4 -O-CO-NH-(CH 2) 2 ~ |
| С е р у с д е рж а щ е | ||
| Тіоефірна | Полісульфіди | Поліетиленсульфід (~CH 2 -CH 2 -S~) |
| Сульфонова | Полісульфони | Полі- n,n`-оксидифенілсульфон |
Неорганічні гетероцепніполімери являють поліборазол, полікремнієва кислота, поліфосфонітрилхлорид. Елементоорганічні гетероцепні полімери включають велику групу найбільш затребуваних сполук неорганічних ланцюгів з органічними бічними групами. До них відносяться кремнійсодержащие полімери, ланцюги яких складаються з атомів кремнію і кисню, що чергуються ( поліорганосилоксани ) або азоту ( поліорганосилазани ). Полімери з третім гетероатомом в основному ланцюгу – металом називаються поліметалорганосилоксанами (Поліалюмоорганосіл-оксани, поліборорганосилоксани і політитанорганосилоксани). Існують також полімери з органонеорганічними ланцюгами з атомів вуглецю, кремнію, кисню (полікарбосилоксани, полікарбосилани, полікарборани), які можуть містити аліфатичні або ароматичні ланки. Усі атоми у ланках розглянутих полімерів з'єднані хімічними ковалентними зв'язками . Існують також координаційні (хелатні, внутрішньокомплексні) гетероцепні полімери, в яких ланки з'єднані донорно-акцепторною взаємодією з іоном металу, що утворює координаційний зв'язок (побічна валентність) та іонний зв'язок (Головна валентність). Хімічні та металеві зв'язки при довжині 0,1-0,2 нмзначно перевищують за величиною енергії фізичні зв'язки та навіть водневий зв'язок (довжина 0,24-0,32 нм), яка займає проміжне положення між фізичними та хімічними зв'язками. Від хімічної будови та складу ланок залежить і полярність зв'язків, яку кількісно оцінюють величиною дипольного моменту про, Рівного добутку заряду на відстань між зарядами (табл.1.3), а також рівень міжмолекулярної взаємодії в полімері. Залежно від полярності зв'язків полімер може бути полярним і неполярним . Дипольний момент всіх органічних карбоцепних аліфатичних (неполярних) полімерів наближається до нуля. Залежно від будови макромолекул між ними можуть виявлятися дисперсійні, орієнтаційні та індукційні зв'язки. Дисперсійні зв'язки зумовлені виникненням миттєвих диполів в атомах під час обертання електронів навколо ядер. Для полярних макромолекул характерні орієнтаційні (Диполь-дипольні) зв'язки. У полі диполів полярних макромолекул можуть поляризуватися і неполярні макромолекули. Між постійним та наведеним диполями виникають індукційні зв'язку.
Міжмолекулярна взаємодіявизначає здатність полімеру до розчинення в низькомолекулярних рідинах, поведінка при низьких температурах, еластичні та інші властивості. Рівень його вимірюють параметром розчинності - Відношенням добутку щільності полімеру на суму констант тяжіння окремих груп атомів у складовій ланці до молекулярної маси ланки. Для цього використовують також щільність енергії когезії (кДж/моль), яка еквівалентна роботі видалення взаємодіючих макромолекул або груп атомів один від одного на нескінченно великі відстані. При температурі склування Т с енергія міжмолекулярної взаємодії стає вищою за енергію теплового руху, і полімер переходить у твердий засклений стан . Полімери з Тзвище за кімнатну називають пластмасами , а нижче за кімнатну і параметром розчинності 14-19 ( М . Дж/м 3 ) 1/2 – еластомірами (Каучук).
Молекулярна маса полімерів та методи її визначення. Молекулярно-масовий розподіл та форма макромолекул. Класифікація полімерів за кількістю та порядком розташування складових ланок.
Молекулярна маса(ММ) – важлива характеристика структури полімерів, що визначає рівень механічних властивостей і належність до певної групи: олігомери (реактопласти) – 10 3 -10 4 , кристалічні термопласти – 10 4 -5 . 10 4 аморфні термопласти - 5 . 10 4 -2 . 105, каучуки - 105-106. Чим менше ММ полімерів, тим нижче в'язкість їх розплавів і вони формуються легше. Механічні властивості визначаються більше ступенем затвердіння (олігомери) і кристалічності (поліаміди, поліефіри) або переходом в склоподібний стан. Найбільшу ММ мають каучуки, які важко формуються, але вироби мають високу еластичність. Оскільки за великої ММ не виходить однаковий ступінь полімеризації, макромолекули розрізняються за розмірами. Полідисперсність (полімолекулярність) - одне з основних понять у фізикохімії полімерів, а тип молекулярно-масового розподілу (ММР) – важливий показник, що впливає фізико-механічні властивості полімерів не менше, ніж ММ.
Оскільки ММ – середньостатистична величина, різні методи її визначення дають різні значення. З рідньочислові методи засновані на визначенні числа макромолекул у розведених розчинах полімерів, наприклад, шляхом вимірювання їх осмотичного тиску, а середньомасові - на визначенні маси макромолекул, наприклад, шляхом вимірювання світлорозсіювання. Середньочислову ММ ( M n ) отримують простим розподілом маси зразка полімеру на число макромолекул у ньому, а середньомасову ММ: M w = M 1 w 1 +M 2 w 2 +…+M i w i , де w 1 , w 2 , w i - Масові частки фракцій; M 1 , M 2 , M i - Середньомасові ММ фракцій. Середньов'язкова ММ, що наближається до середньомасової ММ, визначається в'язкістю розведених розчинів. Полімер називається монодисперсним якщо складається з однієї фракції з дуже близькими один до одного розмірами макромолекул, і для нього відношення M w/M n = 1,02-1,05. В інших випадках середньомасова ММ більша за середньочислову ММ, а їх відношення ( M w/M n =2,0-5,0) є мірою полідисперсності полімеру. Чим більше M w/M n , Тим ширше ММР. На кривій ММР полімеру значення M n посідає максимум, тобто. на фракцію, частка якої у складі полімеру найбільша, а M w зсунуто вправо по осі абсцис.
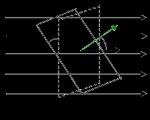
Великі розміри макромолекул полімерів зумовили ще одну особливість їхньої структури. Вони можуть бути лінійними або розгалуженими (З бічними відгалуженнями від основного ланцюга або зіркоподібної форми). За близьких значень ММ вони стають ізомерами . Властивості полімерів, що складаються з макромолекул лінійних та розгалужених, сильно різняться. Розгалуженість - небажаний показник структури макромолекул, що знижує їх регулярність і ускладнює кристалізацію полімеру. Сполука макромолекул хімічними зв'язками призводить до формування сітчастих структур ще більше змінюють властивості полімерів. Відповідно до таких відмінностей щодо будови макромолекул (рис.1.1) і полімери називають лінійними , розгалуженими і сітчастими (пошитими ).
У разі поняття «макромолекула» втрачає сенс, оскільки весь зразок зшитого полімеру стає однією гігантської молекулою. Тому в пошитих полімерах визначають середнє значення ММ відрізка ланцюга між хімічними зв'язками (вузлами сітки), що з'єднують макромолекули.
Сополімеримістять в основному ланцюгу ланки двох і більше різних мономерів (наприклад, бутадієн-стирольний каучук) і мають більш складну будову, ніж гомополімери , що складаються з ланок одного мономеру Сополімер з безладним з'єднанням ланок мономерів у макромолекулі називають статистичним , з правильним їх чергуванням – чергуються , а з великою протяжністю ділянок (блоків) з ланок одного мономеру - блок-сополімером . Якщо блоки одного з мономерів приєднані до основного ланцюга макромолекули, складеної з ланок іншого мономеру, у вигляді великих бічних відгалужень, то кополімер називають щепленим . Структура сополімеру характеризується хімічним складом і довжиною блоків або щеплених ланцюгів та числом блоків або щеплень у макромолекулі. Ланки однакових чи різних мономерів можуть з'єднуватися регулярно (кінець одного - початок іншого) або нерегулярно (кінець одного – кінець іншого, початок іншого – початок третьої ланки, та ін.), а заступники у бічних групах можуть мати регулярне чи нерегулярне просторове розташування. Структуру макромолекули визначають також її конфігурація та конформація.
Конфігурація макромолекул та стереоізомери. Конформація та гнучкість макромолекул. Гнучколанцюгові та жорстколанцюгові полімери та форма їх макромолекул.
Конфігурація макромолекули– це певне просторове розташування її атомів, яке не змінюється при тепловому русі, внаслідок чого різні її види є стабільними ізомерами. Цис-ізомери характеризуються розташуванням різних заступників по різні боки від подвійного зв'язку в кожній ланці, що повторюється, а транс-ізомери - Наявністю різних заступників по один бік від подвійного зв'язку. Прикладом таких ізомерів є НК та гуттаперча – ідентичні за хімічною будовою природні поліізопрени. Гутаперча є пластмасою з кристалічною структурою, що плавиться при 50-70 О С, а НК - еластомером в інтервалі температур від +100 проЗ до -72 проЗ, тому що їх макромолекули мають різні періоди ідентичності . У цис-поліізопрене (НК) орієнтовані в одному напрямку метильні групи зустрічаються через одну складову ланку, що дорівнює 0,82 нм, а в його транс-ізомері (гуттаперче) – через 0,48 нм:
цис- 1,4-поліізопрен (НК)
транс-1.4-поліізопрен
З макромолекул оптичних полімерів з асиметричним атомом вуглецю спеціальними методами синтезу отримують стереорегулярні ізомери - ізотактичні (заступники - по один бік площини макромолекули) та синдіотактичні (заступники - з різних боків):
Вони відрізняються за властивостями від атактичних полімерів з нерегулярним розташуванням замісників. Взаємне відштовхування заступників призводить до їх зміщення щодо один одного в просторі, і тому площина симетрії згинається у вигляді спіралі. Структура спіралей характерна і біологічно активних полімерів (наприклад, подвійна спіраль ДНК). Структура макромолекул стереоізомерів є носієм інформації про способи їх синтезу, а в білках подвійні спіралі ДНК несуть величезну інформацію про їх біологічну спадковість.
Конформація макромолекули- це просторове розташування атомів чи груп атомів, що може змінюватися під впливом теплового руху без руйнації хімічних зв'язків з-поміж них. Велика довжина макромолекули при можливості обертання її частин навколо хімічних зв'язків обумовлює поворотну ізомерію , що виражається у виникненні різних конформацій. Чим ближче один до одного знаходяться атоми водню. цис-положення), тим більше їх відштовхування і потенційна енергія макромолекули. Взаємодія посилюють полярні замісники, наприклад, атоми хлору. У транс-ізомерах потенційна енергія макромолекули менше, розташування атомів вигідніше, ніж у цис-ізомери. Енергетичний бар'єр обертання частин макромолекули, що робить його загальмованим , що складається з низки коливань, допомагають подолати флуктуації теплової енергії . Сукупність коливань та переміщень навколо простих зв'язків наводить до викривлення макромолекули в просторі, який може йти в різних напрямках і змінюватись у часі. Іншими словами, макромолекула має гнучкістю - Здатністю до зміни своєї конформації в результаті теплового руху або дії зовнішніх сил. При великій кількості атомів ланцюг може не просто викривлятися, а навіть згортатися у дуже пухкий макромолекулярний клубок , розмір якого можна охарактеризувати середньоквадратичною відстанню між її кінцями і розрахувати математично, знаючи число складових ланок у ній. Через ланцюгову структуру макромолекул переміщення одного атома або угруповання призведе до переміщення та інших, внаслідок чого виникає рух, подібний до переміщення гусениці або черв'яка, який називається рептаційним (Рис.1.2). Відрізок ланцюга, що переміщається як єдине ціле в елементарному акті руху, називається сегментом ланцюга . Термодинамічна гнучкість характеризує здатність ланцюга змінювати свою конформацію під дією теплового руху та може бути оцінена параметром жорсткості, довжиною термодинамічного сегмента або параметром гнучкості Флорі. Чим менші ці показники, тим вища ймовірність переходу макромолекули з однієї конформації до іншої (табл.1.4). Параметр жорсткості оцінюють ставленням середньоквадратичних відстаней між кінцями реальної та вільно-зчленованої ланцюгів у розведених розчинах полімеру. Довжина термодинамічного сегмента А (сегмент Куна) характеризує таку послідовність ланок, при якій кожна ланка поводиться незалежно від інших, і також пов'язана з середньоквадратичною відстанню між кінцями ланцюга. Вона дорівнює гідродинамічній довжині макромолекули для гранично жорстких і довжині ланки, що повторюється, для гранично гнучких ланцюгів. Полімери дієнового ряду та зі зв'язками ~Si-O~ або ~C-O~ в основному ланцюгу характеризуються більшою гнучкістю в порівнянні з полімерами вінілового ряду, тому що у них через зменшення обмінних взаємодій між СН 2 -групами в 100 разів нижче за енергію поворотних ізомерів. Природа заступників мало впливає гнучкість макромолекул. Параметр гнучкості Флорі f пропоказує вміст гнучких зв'язків у макромолекулі та служить критерієм гнучкості, за яким полімери ділять на гнучколанцюгові (f про>0,63; А<10нм) та жорстколанцюгові (f про<0,63; А>35нм). Останні не бувають у конформації макромолекулярного клубка та мають витягнуту форму макромолекул – пружної струни (поліалкілізоціанат, А =100), колінчастого валу (полі- п-бензамід, А =210) або спіралі (біополімери, А =240).Кінетична гнучкість макромолекули відображає швидкість її переходу в силовому полі з однієї конформації до іншої і визначається величиною кінетичного сегменту , тобто. тієї частини макромолекули, що відкликається на зовнішній вплив як єдине ціле. На відміну від термодинамічного сегмента, він визначається температурою та швидкістю зовнішнього впливу. З підвищенням температури зростають кінетична енергія та гнучкість макромолекули та зменшується величина кінетичного сегмента. У разі, коли час дії сили більше, ніж час переходу з однієї конформації в іншу, кінетична гнучкість висока, а кінетичний сегмент за величиною наближається до термодинамічного сегменту. При швидкій деформації кінетичний сегмент близький до гідродинамічної довжини макромолекули, і навіть термодинамічно гнучкий ланцюг поводиться як жорсткий. Кінетична гнучкість ізольованої макромолекули визначається за в'язкопружними властивостями сильно розведених розчинів з подальшою їхньою екстраполяцією до нульової коцентрації. Макромолекули гнучколанцюжного аморфного полімеру мають клубкоподібну форму як ізольованому вигляді, і у масі. При цьому структура полімеру не схожа на структуру «молекулярної повсті», в якій макромолекули переплутані хаотично, як вважали раніше. Ідея про впорядковані області в аморфних полімерах висловлена 1948 р. Алфреєм.
конфігурація макромолекули інакшепервинна структура(англ.) - просторове розташування атомів у . Визначається значеннями валентних кутів та довжинами відповідних зв'язків.
Опис
Конфігурація макромолекули визначається взаємним розташуванням мономерних ланок, що входять до неї, а також їх структурою. В даний час для опису конфігурації макромолекул зазвичай використовують термін «структура» або «первинна структура».
Розрізняють ближній (конфігурація приєднання сусідніх ланок) та далекий конфігураційний порядок, що характеризує структуру досить протяжних ділянок макромолекул. Кількісним заходом тактовності (порядку) є ступінь стереорегулярності. Крім цього, тактовність може описуватися кількістю різних типів пар найближчих сусідів (ді-, три-, зошит), розподіл яких визначається експериментально. Кількісною характеристикою конфігурації статистичних сітчастих макромолекул, наприклад, є щільність зшивки, тобто середня ділянка ланцюга між вузлами сітки.
Конфігурацію макромолекул визначають методами рентгеноструктурного аналізу, подвійного променезаломлення та ін. Як правило, кожен метод найбільш «чутливий» до будь-якої конфігураційної характеристики; так, ЯМР у багатьох випадках дозволяє кількісно характеризувати ближній конфігураційний порядок
· органічні полімери(До складу входять органогенні елементи - С, N, O, P, S). Діляться на гомоцепні (в основному ланцюгу містяться тільки атоми вуглецю) і гетероцепні (до складу основного ланцюга входять інші атоми) До цього класу полімерів відносяться біополімери.
· елементоорганічні полімери(У складі основного ланцюга поряд з атомами вуглецю знаходяться атоми Si, Al, Ti, Ge, B).
· неорганічні полімери (в основний ланцюг не містяться атоми вуглецю, наприклад силікони).
1. Перерахуйте види номенклатури полімерів.
2. Як формується номенклатура, що ґрунтується на назві мономерів?
3. Наведіть приклади назв полімерів за номенклатурою, заснованою на хімічній структурі полімерного ланцюга.
4. Назвіть типи класифікації полімерів. Наведіть приклади.
5. Які існують види кополімерів?
6. Як здійснюється хімічна класифікація полімерів?
Завдання для самостійного вирішення *
2. Класифікація та структурні формули основних полімерів
2.1 Класифікація полімерів
Вопросы2501 – 2502, 2403 – 2406, 2307
2.2. Структурні формули основних полімерів
Запитання 3501, 3402, 3303 - 3309
*Тут і надалі завдання наведені з «Збірника тестових завдань для тематичного та підсумкового контролю з дисципліни «Хімія та фізика полімерів»,М.,МІТХТ, 2009р.
Розділ №3. Основні характеристики макромолекул
Макромолекули характеризуються 4 основними параметрами:
1. Молекулярна маса (ММ), молекулярно – масовий розподіл (ММР);
2. Зміна макромолекули;
3. Конформація макромолекули;
4. Топологія (лінійні, розгалужені).
· ММ дозволяє визначити довжину, розміри макромолекул;
· Конфігурація визначає хімічну будову макромолекул;
· Конформація визначає форму макромолекул.
3.1. Молекулярна маса (ММ), молекулярно-масовий розподіл (ММР)
Основні відмінності поняття ММ для ВМС та НМС:
ММ є мірою довжини молекули для лінійних полімерів і може бути виражена через ММ низькомолекулярних складових ланок, що повторюються:
https://pandia.ru/text/78/135/images/image040_18.gif" m0 - молекулярна маса складової повторюваної ланки;
Pn – ступінь полімеризації
Більшість синтетичних полімерів не є індивідуальними сполуками, а складаються із суміші молекул різного розміру, але однакового складу.
Це призводить до того, що:
· У полімерів ефективна молекулярна маса є середньою величиною через полідисперсність - розкиду макромолекул за величиною ММ;
· У більшості полімерів кінцеві групи відрізняються від складу ланок полімерного ланцюга;
· У макромолекулах можуть існувати певні бічні відгалуження, це також розрізняє макромолекули один від одного;
· більшість біополімерів – індивідуальні сполуки (кожен конкретний полімер – унікальний за складом, будовою та молекулярною масою).
Причини полідисперсності:
1. через статистичний характер процесу отримання полімеру: у процесі синтезу виходять макромолекули різної довжини;
2. через перебіг процесів часткової деструкції макромолекул, наприклад, в ході експлуатації матеріалу;
3. через відмінність кінцевих груп у молекули полімеру;
4. через наявність у деяких полімерів відгалужень у різних місцях та різної хімічної структури.
3.1.1. Способи усереднення молекулярних мас
1) Усереднення за кількістю молекул
Середньочислова ММ:
Мw=∑(Ni Mi2)/∑(NiMi) (3.1.1.2)
Враховується маса фракції цієї молекулярної маси.
Mw визначають за допомогою методів хроматографії, ультрацентрифугування, світлорозсіювання.
Kn=Mw/Mn (3.1.1.3)
Для монодисперсних полімерів Kn=1.
При вузькому розподілі Kn=1,01÷1,05.
У промисловості найчастіше отримують полімери з Kn=3÷10.
3) Середньов'язкова ММ:
M = = ((NiMi)1+α/∑(NiMi))1/α, 0<α<1 (3.1.1.4)
![]()
3.1.2. Молекулярно – масовий розподіл (ММР)
Найбільш повною характеристикою молекулярних мас полімерів є функції розподілу молекулярних мас.
Азот, бір, алюміній можуть бути елементами макромолекулярних ланцюжків в інших складових полімерної структури, або входити як гетероатоми в основний ланцюг.

4.3. Вуглець
Має високу схильність до утворення міцних ковалентних зв'язків, як між власними атомами, так і з іншими атомами.
https://pandia.ru/text/78/135/images/image064_12.gif" width="102" height="92"> - двомірна вуглець-вуглецева структура графена, графіту та сажі
Можливе одержання і лінійного ланцюга з атомів вуглецю:
https://pandia.ru/text/78/135/images/image066_10.gif" width="238" height="14 src=">
При нагріванні він перетворюється на графіт.
Набагато великі можливості щодо побудови лінійних макромолекул з атомів вуглецю відкриваються, коли 1 або 2 валентності вуглецю насичуються іншими атомами чи групами.
 - поліетилен
- поліетилен
 - поліпропілен
- поліпропілен
![]() - політетрафторетилен
- політетрафторетилен
Також у складі основного ланцюга можуть бути різні угруповання, що містять гетероатоми:
https://pandia.ru/text/78/135/images/image071_11.gif" width="93" height="43 src="> - складно-ефірне угруповання
https://pandia.ru/text/78/135/images/image073_9.gif" width="105" height="45 src="> - карбамідне (сечовинне) угруповання
https://pandia.ru/text/78/135/images/image076_9.gif" width="185 height=84" height="84">
Але вони хімічно не дуже стійкі і при окисленні кремнію зв'язується з киснем, утворюючи дуже міцні зв'язки кремній-кисень.
У природі кремній зустрічається у вигляді кварцу:

Це жорстка тривимірна структура, яка не виявляє полімерних властивостей лінійних макромолекул. Лінійні макромолекули отримують, замінивши дві валентності кожного атома кремнію на органічні радикали (CH3-, C2H5- і т. д.). При цьому з'являються кремній-органічні полімери.
Можна синтезувати кремнійвмісні полімери:
 - полісилоксани
- полісилоксани
У ланцюг можуть вбудовуватися атоми Al, B, Ti, Zn та інших.
4.5. Фосфор
Атоми фосфору можуть утворювати полімери, але до складу основного ланцюга повинні входити інші атоми (найчастіше кисень):
 - поліфосфати
- поліфосфати
 - поліфосфорна кислота
- поліфосфорна кислота
Залишки ортофосфорної кислоти входять у природні полімери (нуклеїнові кислоти, ДНК та РНК):

Таким чином, двох або полівалентні атоми (C, O, P, N, S, Si, Al, B та деякі інші) можуть бути у вигляді елементів основного ланцюга макромолекул або перебувати в бічних фрагментах; одновалентні атоми (H, F, Cl, J, Br та деякі інші) можуть вибудовуватися тільки як заступники.
Хімія полімерів побудована на основі цих елементів.
4.6. Види полімерів
Полімери отримують або синтетично, або витягують з живих організмів (біополімери), або обробкою вже виділених природних полімерів.
Частина синтетично створених полімерів існує у природі. Полімери виходять з мономерів - низькомолекулярних речовин або в результаті перетворень готових полімерів (синтетичних або природних) - полімер аналогічні перетворення.

1,4-цис-полібутадієну в природі не існує, одержують синтетично з бутадієну.

1,4-цис-поліізопрен існує в природі (натуральний каучук), але в природі синтезується з глюкози та інших речовин (але не з ізопрену, як у промисловості)

Цей поліефір можна отримати конденсацією полі-β-гідроксибутирату, у той же час він синтезується і поряд бактерій.
Синтези біополімерів у цьому курсі не розглядатимуться.
Багато природних полімерів дуже складно отримати синтетично. Вони виходять у живих організмах внаслідок перебігу складних біохімічних реакцій.
Найважливіші природні полімери:
Прикладами можуть бути реакції поліетерифікації:
HO-R-COOH + HO-R-COOH > HO-R-COO-R-COOH + H2O і т.д.
поліамідування:
H2N-R-NH2 + ClOC-R"-COCl > H2N-R-NHCO-R"-COCl + HCl і т.д.
При цьому на відміну від полімеризації елементарний склад продуктів поліконденсації в даному випадку не збігається зі складом мономерних сполук, тому що кожен хімічний акт поліконденсації супроводжується виділенням молекули низькомолекулярного продукту.
Наведеній вище загальній схемі поліконденсації відповідають деякі різновиди процесів, які не супроводжуються виділенням низькомолекулярних продуктів. До них, наприклад, відноситься синтез поліуретанів з гліколей і діізоціанатів:
А-R-OH + O=C=N-R"-N=C=O > HO-R-О-CO-NH-R"-N=C=O і т.д.
Подібні поліконденсаційні процеси часто називають поліприєднанням. По кінетичних закономірностей реакції поліприєднання дуже схожі з реакціями поліконденсації. В обох типах поліконденсаційних процесів зростання макромолекул здійснюється шляхом взаємодії функціональних груп молекул мономерів або таких же груп, що знаходяться на кінцях ланцюгів, що вже утворилися, різної молекулярної маси. Проміжні полімерні продукти, що отримуються в результаті цих реакцій, цілком стійкі і можуть бути виділені у вільному вигляді. Однак вони містять на кінцях реакційні групи і тому здатні до подальших реакцій конденсації, як один з одним, так і з відповідними мономерними молекулами. Звідси випливає, що теоретично поліконденсація може вважатися завершеною лише тоді, коли прореагують всі кінцеві функціональні групи, у результаті має утворитися одна гігантська циклічна макромолекула. Насправді, однак, це ніколи не досягається.
Питання для самостійного опрацювання:
1. Які елементи Періодичної системи здатні до утворення полімерних кіл?
2. Наведіть приклади полімерів, які одержують синтетично.
3. Наведіть приклади природних полімерів.
4. Які мономери можуть брати участь у реакції полімеризації?
1.3. Конфігурація макромолекул
Поняття конфігурації включає певне просторове розташування атомів макромолекул, яке змінюється при тепловому русі. Перехід від однієї конфігурації в іншу неможливий без розриву хімічних зв'язків.
Розрізняють : 1) конфігурацію ланки, 2) ближній порядок – конфігурацію приєднання ланок, 3) далекий порядок – конфігурацію великих ділянок (наприклад, блоків та його чергування, чи довжину і розподіл розгалужень), 5) конфігурацію витягнутого ланцюга загалом.
Конфігурація ланки. Прикладами є цис-і транс-конфігурації у дієнових полімерів
1,4-цис-поліізопрен 1,4-транс-поліізопрен (натуральний каучук) (гуттаперча) Іншим прикладом може бути l,d-ізомерія. Наприклад,
для полімерів зі ланками ~СН2 –СНR~, де R – будь-який радикал, можливе утворення двох ізомерів: l – лівообертальний, а d – правообертальний
Конфігурація приєднання ланок(Ближній порядок). Ланки в ланцюгу можуть приєднуватися на кшталт «голова до хвоста» і «голова до голови»:

є приєднання типу «голова до хвоста», а приєднання типу «голова до голови» вимагає подолання великих активаційних бар'єрів.
Для кополімерів типи структурних ізомерів збільшуються порівняно з гомополімерами. Наприклад, для кополімерів бутадієну та стиролу можливо:
1. послідовне чергування ланок –А–В–А–В–А–В– ,
2. поєднання ланок у вигляді діад та тріад-АА-ВВВ-АА-ВВВ-,
3. статистичне поєднання ланок-АА-В-АА-ВВВ-А-В-. Далекий конфігураційний порядокпоширюється на
десятки та сотні атомів в основному ланцюзі. Наприклад, великі послідовності блоків у блок-сополімерах або великі послідовності ланок з однаковою стереорегулярністю (наприклад, полімери з ізотактичною, атактичною та синдіотактичною структурою).
Ізотактичний Атактичний Сіндіотактичний
Конфігурація ланцюга загаломвизначається взаємним розташуванням великих послідовностей ланок (при далекому порядку). Наприклад, для розгалужених макромолекул різні типи конфігурацій показано на рис.4.
Мал. 4. Зміни макромолекул

1.4. Конформація макромолекул
Конформація – це змінний розподіл у просторі атомів чи груп атомів, які утворюють макромолекулу. Перехід з однієї конформації в іншу може відбуватися рахунок обертання, повороту чи коливання ланок навколо одинарних зв'язків під впливом теплового руху чи зовнішніх сил і супроводжується розривом хімічних зв'язків.
Полімери можуть приймати різні конформації:
Статистичний клубок– це згорнута конформація. Утворюється, коли інтенсивність внутрішнього теплового руху переважає зовнішній вплив. Характерна лінійним полімерам [ПЕ, ПП, ПБ, ПІБ та сходовим полімерам (поліфеніленсилоксан).
Спіраль - утворюється у полімерів рахунок Н-зв'язків (наприклад, у білкових молекул і нуклеїнових кислот).
Глобула – дуже компактна частка формою близька до сферичної. Характерна полімерам із сильною внутрішньомолекулярною взаємодією (наприклад, у ПТФЕ).
Стрижень або струна виявлена у алкілполіізоціанатів.
Складчаста конформація. Характерна полімерів у кристалічному стані (наприклад, у ПЕ).
Конформація колінчастого валуреалізується у полі-n-бенз-аміду.
Рис.5. Конформація макромолекул
1.5. Гнучкість макромолекул
Гнучкість є однією з найважливіших характеристик полімерів, що визначає високоеластичні, релаксаційні та термомеханічні властивості полімерів, а також особливості властивостей їх розчинів. Гнучкість характеризує здатність макромолекул змінювати свою форму під впливом теплового руху ланок чи зовнішніх механічних впливів. Гнучкість обумовлена внутрішнім обертанням ланок чи частин макромолекул щодо один одного. Розглянемо явище внутрішнього обертання молекулах з прикладу найпростішого органічного сполуки – молекули етану.
У молекулі етану (СН3 –СН3 ) атоми вуглецю пов'язані з атомами водню та один з одним ковалентними (σ–зв'язками), причому кут між напрямками σ–зв'язків (валентний кут) становить 1090 28/ . Це викликає тетраедричне розташування заступників (атомів водню) у просторі молекули етану. Внаслідок теплового руху в молекулі етану відбувається обертання однієї групи СН3 щодо іншої навколо осі С-С. При цьому безперервно змінюється просторове розташування атомів та потенційна енергія молекули. Графічно різні крайні розташування атомів у молекулі можна як проекцій молекули на горизонтальну площину (Рис.6). Припустимо, що у положенні а потенційна енергія молекули дорівнює U1 , а положенні б – U2 , у своїй U1 ≠ U2 , тобто. становища молекули енергетично нерівноцінні. Становище б , у якому атоми Н розташовані друг під одним, є енергетично невигідним, оскільки між атомами Н виявляються сили відштовхування, які прагнуть перевести атоми в енергетично вигідне становище а . Якщо прийняти
U1 = 0, то U2 = max.

Мал. 6. Проекційні формули крайніх розташування атомів Н у просторі в молекулі етану.
Мал. 7. Залежність потенційної енергії молекули від кута повороту метильної групи.
При повороті однієї групи СН3 щодо іншої на 600 молекула зі становища а перетворюється на бі далі через 600 знову у становище і т.д. Зміна значень потенційної енергії молекули етану від кута повороту показано на рис.7. Молекули з меншою симетрією (наприклад, молекула дихлоретану) мають складнішу залежність U=f(φ).
Потенційним (U 0 ) або активаційним бар'єром обертово-
ня називається енергія, необхідна для переходу молекули зі становища мінімуму в положення максимуму потенційної енергії. Для етану U0 мала величина (U0 = 11,7 кДж/моль) та при
звичайній температурі відбувається обертання груп СН3 навколо зв'язку З-З великою швидкістю (1010 об/сек).
Якщо молекула має запас енергії менший U0, то обертання відсутнє і відбувається лише коливання атомів щодо положення мінімальної енергії – це обмежене або
загальмоване обертання.
У полімерів внаслідок внутрішньо-і міжмолекулярних взаємодій залежність U=f(φ) має складну форму.
Якщо одне становище ланки ланцюга характеризується потенційної енергією U1 , інше – U2 , то енергія переходу з одного становища до іншого дорівнює різниці ∆U= U1 – U2 . Різниця енергій переходу ∆U з одного рівноважного положення ланки макромолекули до іншого характеризує термодинамічну гнучкість. Вона визначає здатність ланцюга згинатися під впливом теплового руху.
Іншою характеристикою гнучкості є швидкість переходу ланок з одного положення до іншого. Швидкість конформаційних перетворень залежить від співвідношення величини U0 та енергії зовнішніх впливів. Чим більше U0, тим повільніше повороти ланок і менше гнучкість. Гнучкість макромолекул, що визначається величиною U0 називається кінетичної гнучко-
Чинники, що визначають гнучкість макромолекул
До таких факторів відносять: величину U0, ММ полімеру, густоту просторової сітки, розмір замісників та температуру.
Потенційний бар'єр обертання (U 0). Величина U0 залежить від внутрішньо-і міжмолекулярних взаємодій. Розглянемо фактори, що впливають на U0 та гнучкість ланцюгів у карбоцепних полімерів.
Карбоцепні полімери
У карбоцепних полімерів найменш полярними є граничні вуглеводні. У них внутрішньо- і міжмолекулярні взаємодії невеликі, а також малі значення U0 і ∆U, отже полімери мають велику кінетичну і термодинамическую гнучкість. Приклади: ПЕ, ПП, ПІБ.
Особливо низькі значення U0 у полімерів, в ланцюзі яких поруч із ординарною є подвійний зв'язок.
-СН2 -СН = СН-СН2 - Полібутадієн Введення в макромолекули заступників, що містять по-
лярні групи призводить до внутрішньо-і міжмолекулярних взаємодій. При цьому суттєво впливають ступінь полярності
При введенні полярних груп можливі три випадки впливу на гнучкість:
1. Полярні групи близько розташованіі можливі з-поміж них сильні взаємодії. Перехід такими полімерами з одного просторового положення в інше вимагає подолання великих U0 тому ланцюги таких полімерів найменш гнучкі.
2. Полярні групи розташовані в ланцюзі рідкота взаємодії між ними не виявляються. Значення U0 та ∆U невеликі та полімери мають велику кінетичну та термодинамічну гнучкість.

-СF 2 -СF 2 -
Приклад: Поліхлоропрен
3.Полярні групи розташовані так, що електричні поля взаємно компенсуються. У цьому сумарний дипольний момент макромолекули дорівнює нулю. Тому низькі значення U0 і ∆U та полімери мають велику кінетичну та термодинамічну гнучкість.
Приклад: Політетрафторетилен
Гетероцепні полімери
У гетероцепних полімерів обертання можливе навколо зв'язків С–О, С–N, Si–O, C–C. Значення U0 для цих зв'язків невеликі і ланцюги мають достатню кінетичну гнучкість. Приклади: поліефіри, поліаміди, поліуретани, силоксанові каучуки.
Однак гнучкість гетероцепних полімерів може обмежуватися міжмолекулярними взаємодіями за рахунок утворення Н-зв'язків (наприклад, целюлози, поліамідів). Целюлоза є одним із жорстколанцюгових полімерів. У неї міститься велика кількість полярних груп (-OH) і тому для целюлози характерні внутрішньо-і міжмолекулярні взаємодії та високі значення U0 та мала гнучкість.
Молекулярна маса полімеру. Збільшення ММ полімеру підвищує згорнутість ланцюга і тому довгі макромолекули
мають більшу кінетичну гнучкість порівняно з короткими макромолекулами. У міру збільшення ММ зростає кількість конформацій, яка може приймати макромолекула та гнучкість ланцюгів збільшується.
Густота просторової сітки. Що більше хімічних зв'язків між макромолекулами, то менше гнучкість ланцюгів, тобто. із збільшенням густоти просторової сітки гнучкість зменшується. Прикладом є зниження гнучкості ланцюгів зі збільшенням числа зшивок у ряді резол< резитол<резит.
Вплив розміру та кількості заступників. Збільшення числа полярних і великих за розміром замісників знижує рухливість ланок макромолекули та зменшує кінетичну гнучкість. Прикладом є зниження гнучкості макромолекул кополімеру бутадієну та стиролу зі збільшенням вмісту громіздких фенільних замісників у ланцюзі.
Якщо при одному атомі вуглецю в основному ланцюгу полімеру є два замісники (наприклад, ОСН3 і СН3 у ланках ПММА), то макромолекула стає кінетично жорсткою.
Температура. З підвищенням температури збільшується кінетична енергія макромолекули. Доки величина кінетичної енергії менше U0 , ланцюги здійснюють крутильні коливання. Коли кінетична енергія макромолекули стає рівною чи перевищує величину U0 ланки починають обертатися. З підвищенням температури величина U0 мало змінюється, а швидкість повороту ланок збільшується та кінетична гнучкість зростає.
Контрольні питання
1 Загальні відомості про полімери, поняття, визначення.
2 Дайте визначення та наведіть приклади органічних, не-
органічних та елементоорганічних полімерів.
2 Класифікація гомоланцюгових полімерів, приклади.
3 Класифікація гетероланцюгових полімерів, приклади.
4 Термодинамічна та кінетична гнучкість макромолекул. Які чинники впливають на гнучкість макромолекул?
5 Що таке конфігурація макромолекул та які можливі різновиди конфігурації макромолекул? приклади.
6 Що таке конформація макромолекул та які можливі різновиди конформацій макромолекул? приклади.
7 Якими параметрами характеризують молекулярну масу,молекулярно-масовий розподіл та полідисперсність полімерів?
8 Молекулярні властивості олігомерів.
9 Фракціонування полімерів та побудова кривих моле-кулярно-масового розподілу.
В межах заданої конфігурації в макромолекулі є велика кількість внутрішніх ступенів свободи, пов'язаних із обертанням навколо осі одинарних зв'язків основного ланцюга. Як наслідок, макромолекула здатна набувати різних форм ( конформації), тобто. для полімерів характерна конформаційна ізомерія.
Конформація - це просторове розташування атомів та атомних груп, яке може бути змінено без розриву хімічних зв'язків основної ціни внаслідок теплового руху та (або) зовнішніх впливів.
Нижче схематично зображено механізм зміни конформації ізотактичної тріади вінілового полімеру в результаті повороту на 180° навколо З-З-зв'язку. Очевидно, що подібні конформаційні переходи не супроводжуються зміною заданої конфігурації та розривом хімічних зв'язків.
Таким чином, конформаційна ізомерія макромолекул визначається внутрішнім обертанням навколо одинарних хімічних зв'язків полімерної ланцюгової конструкції.
Основні положення конформаційної ізомерії макромолекул
Розглянемо основні закономірності внутрішнього обертання навколо хімічних зв'язків на прикладі низькомолекулярної моделі - 1,2-дихлоретан.

Внаслідок взаємодії бічних заступників (Ні С1) при повному повороті навколо осі-С-С-зв'язку на 360 ° в молекулі 1,2-дихлоретану послідовно реалізується ряд різних поворотних ізомерів, або конформерів,з певною потенційною енергією. Графічно це можна у вигляді енергетичної карти - залежності потенційної енергії конформера від кута повороту. Для 1,2-дихлоретану подібна карта схематично зображена на рис. 1.3.

Мал. 1.3.Залежність потенційної енергії Uвалентно не пов'язаних атомів молекули 1,2-дихлоретан від кута повороту
У молекул подібного типу розрізняють три стабільні конформації: одна транс-та дві гош-конформації (від фр. gauche- косий, перекошений), що відповідають мінімумам потенційної кривої. Максимуми відповідають нестабільним заслінним конформаціям, зокрема г^іс-конформеру.
У полімерах внутрішнє обертання навколо одинарних зв'язків має низку специфічних особливостей проти низькомолекулярними сполуками. Розглянемо фрагмент ланцюга поливинилхлорида у конфігурації «голова – голова».

На відміну від 1,2-дихлоретану, у виділеному фрагменті замість двох атомів II замісниками у вуглецевих атомів є продовження полімерного ланцюга -СН 2 -. Іншими словами, при обертанні навколо зв'язку між г-м та (г + 1)-м вуглецевими атомами (г + 2)-й атом вуглецю з подальшим продовженням ланцюга відіграє роль заступника (рис. 1.4).

Мал. 1.4.
Положення (г + 2)-го атома щодо попереднього зв'язку задано основою конуса з урахуванням валентного кута 0. Однак поворот па 360° можливий лише при переміщенні у просторі протяжного продовження ланцюга, що потребує величезної теплової енергії, що перевищує, як правило, енергію дисоціації хімічних. зв'язків. В результаті внутрішнє обертання в полімерах є загальмованимта реалізується в межах певної дуги кола. Розмір цієї дуги визначає кут загальмованого внутрішнього обертання ф.Величина кута загальмованого внутрішнього обертання залежить від температури, природи хімічного зв'язку, полярності та обсягу замісників, конфігураційного складу полімеру тощо.
Таким чином, у першому наближенні, внутрішнє обертання полімерних ланцюгах зводиться до поворотів кожного наступного зв'язку щодо попередньої. Насправді ці події мають яскраво виражений кооперативний характер, оскільки обертання двох сусідніх зв'язків щодо одне одного багато в чому визначається як аналогічними процесами в ближньому оточенні, і взаємодіями далекого порядку. У зв'язку з цим у разі полімеру кут загальмованого внутрішнього обертання є усередненою величиною. Кількісні оцінки цієї характеристики будуть наведені нижче.