मॅक्रोमोलेक्यूल्स आणि स्टिरिओइसॉमर्सचे कॉन्फिगरेशन. मॅक्रोमोलेक्यूल्सची रचना आणि लवचिकता
मुख्य शृंखला आणि संपूर्ण मॅक्रोमोलेक्यूलच्या रासायनिक संरचनेनुसार पॉलिमरचे वर्गीकरण. पॉलिमरमधील इंटरमॉलिक्युलर परस्परसंवाद. संयोग ऊर्जा घनता आणि विद्राव्यता मापदंडाच्या संकल्पना.
मॅक्रोमोलेक्यूल्सची रचनात्यांची रासायनिक रचना आणि लांबी, लांबीचे वितरण आणि आण्विक वजन, आकार आणि एककांची अवकाशीय व्यवस्था यांचा समावेश होतो. मुख्य साखळीच्या रासायनिक संरचनेवर आधारित, ते वेगळे केले जातात homochain (कार्बन अणूंच्या साखळीसह - कार्बन साखळी ) आणि heterochain पॉलिमर, आणि संपूर्णपणे मॅक्रोमोलेक्यूल्सच्या रासायनिक संरचनेच्या दृष्टीने - पॉलिमर:
· सेंद्रिय - साखळीमध्ये कार्बन, ऑक्सिजन, नायट्रोजन आणि सल्फर अणू असतात;
· ऑर्गेनोएलमेंट - साखळीमध्ये सिलिकॉन, फॉस्फरस आणि इतर अणू असतात ज्यात कार्बन अणू किंवा गट जोडलेले असतात किंवा त्याउलट;
· अजैविक - साइड ग्रुपशिवाय अनेक (दुहेरी किंवा तिहेरी) बंध असलेले कार्बन अणू किंवा कार्बन चेन अणू पूर्णपणे नाहीत.
एकदम साधारण सेंद्रिय कार्बन साखळी पॉलिमर, त्यांच्या विविध डेरिव्हेटिव्ह्जसह (हॅलोजन-युक्त, इथर, अल्कोहोल, ऍसिड इ.), ज्याचे नाव "पॉली" उपसर्ग असलेल्या मोनोमरच्या नावाने तयार केले जाते. संतृप्त अॅलिफॅटिक कार्बन-चेन पॉलिमरमध्ये पॉलिथिलीन, पॉलीप्रॉपिलीन, पॉलीव्हिनिल क्लोराईड, पॉलीटेट्राफ्लुरोइथिलीन, पॉलीट्रिफ्लुरोक्लोरोइथिलीन, पॉलीव्हिनिल अल्कोहोल, पॉलीव्हिनिल एसीटेट, पॉलीएक्रिलामाइड, पॉलीएक्रिलोनिट्रिल, पॉलीमिथाइल मेथाक्रिलेट आणि इतर समाविष्ट आहेत. पॉलीबुटाडीन, पॉलिसोप्रीन आणि पॉलीक्लोरोप्रीन असंतृप्त आहेत, फॅटी सुगंधी पॉलिमरचे उदाहरण म्हणजे पॉलिथिलीनफेनिलिन आणि सुगंधी पॉलिमर पॉलिफेनिलिन आहेत. क्रमांक अजैविक होमोचेन पॉलिमर मर्यादित आहेत - कार्बन-चेन कार्बिन (~C≡C-C≡C~) आणि कम्युलिन (=C=C=C=), तसेच पॉलिसल्फर (~S-S-S~), पॉलिसिलेन (~SiH) 2 -SiH 2 ~), पॉलिगरमन (~GeH 2 -GeH 2 ~), इ. अधिक सामान्य ऑर्गोएलिमेंट होमोचेन ऑर्गेनिक साखळ्यांपासून (कार्बोचेन) ऑर्गेनोएलिमेंट साइड ग्रुप्स किंवा सेंद्रिय रॅडिकल्स असलेल्या अजैविक साखळ्यांपासून बनविलेले पॉलिमर: पॉलीव्हिनिलालकाइल्सिलनेस, पॉलीऑर्गॅनोसिलेन, बोरॉन-युक्त पॉलिमर. सेंद्रिय हेटरोचेन मुख्य साखळीतील कार्यात्मक गटांच्या स्वरूपावर अवलंबून पॉलिमर वर्गांमध्ये विभागले जातात. कार्यात्मक गटांमधील हायड्रोकार्बन गटांच्या संरचनेवर अवलंबून, ते अॅलिफॅटिक किंवा सुगंधी असू शकतात (तक्ता 1.1).
तक्ता 1.1.
विविध वर्गांचे हेटरोचेन पॉलिमर:
| कार्यात्मक गट | पॉलिमर | |
| वर्गाचे नाव | प्रतिनिधी | |
| ऑक्सिजन युक्त | ||
| साधे इथरियल | पॉलिथर्स | पॉलीमिथिलीन ऑक्साईड (~CH 2 -O~) |
| पॉलिथिलीन ऑक्साईड (~CH 2 -CH 2 -O~) | ||
| एस्टर | पॉलिस्टर | पॉलिथिलीन टेरेफ्थालेट ([-CH 2 -CH 2 -O-OC-Ar-CO-O-]n) |
| Polyarylates ([-OC-R-COO-R`-O-] n) | ||
| पॉली कार्बोनेट ([-O-Ar-CH 2 -Ar-O-CO-O-Ar-CH 2 -Ar-] n) | ||
| नायट्रोजन असलेले | ||
| एसिटल | एसिटल्स | सेल्युलोज (C 6 H 1 0 O 5) n |
| अमाइड | पॉलिमाइड्स (-СО-NН-) | पॉलीहेक्सामेथिलीन अॅडिपामाइड |
| इमिडे | पॉलिमाइड्स | पॉलीपायरोमेलिटिमाइड |
| युरिया | पॉलीयुरिया | पॉलीनोनामेथिलीन युरिया |
| युरेथेन | पॉलीयुरेथेन्स (–HN-CO-O) | ~(CH 2) 4 -O-CO-NH-(CH 2) 2 ~ |
| सल्फर असलेले | ||
| थिओस्टर | पॉलीसल्फाइड्स | पॉलिथिलीन सल्फाइड (~CH 2 -CH 2 -S~) |
| सल्फोनिक | पॉलीसल्फोन्स | पॉली- n,n`-ऑक्सीडिफेनिल सल्फोन |
अजैविक हेटरोचेनपॉलिमर म्हणजे पॉलीबोराझोल, पॉलिसिलिक ऍसिड, पॉलीफॉस्फोनिट्रिल क्लोराईड. ऑर्गेनोइलेमेंट हेटरोचेन पॉलिमरमध्ये सेंद्रिय बाजूंच्या गटांसह अजैविक साखळीतील सर्वात लोकप्रिय संयुगांचा एक मोठा गट समाविष्ट आहे. यामध्ये सिलिकॉन-युक्त पॉलिमरचा समावेश होतो, ज्याच्या साखळ्यांमध्ये पर्यायी सिलिकॉन आणि ऑक्सिजन अणू असतात ( पॉलीऑर्गेनोसिलॉक्सेन ) किंवा नायट्रोजन ( polyorganosilazanes ). मुख्य शृंखलामध्ये तिसरा हेटरोएटम असलेले पॉलिमर - एक धातू - म्हणतात polymetalorganosiloxanes (पॉलिअल्युमिनियम ऑर्गेनोसिलॉक्सेन्स, पॉलीबोरॉन ऑर्गनोसिलॉक्सेन आणि पॉलिटायटेनियम ऑर्गनोसिलॉक्सेन्स). कार्बन, सिलिकॉन, ऑक्सिजन अणू (पॉली कार्बोसिलॉक्सेन, पॉली कार्बोसिलेन, पॉली कार्बोरेन्स) च्या ऑर्गेनोइनऑर्गेनिक साखळ्या असलेले पॉलिमर देखील आहेत ज्यात अॅलिफेटिक किंवा सुगंधी एकके असू शकतात. मानले गेलेल्या पॉलिमरच्या लिंक्समधील सर्व अणू जोडलेले आहेत रासायनिक सहसंयोजक बंध . तसेच आहेत समन्वय (चेलेट, इंट्राकॉम्प्लेक्स) हेटरोचेन पॉलिमर ज्यामध्ये युनिट्स मेटल आयन तयार करून दाता-स्वीकारकर्त्याच्या परस्परसंवादाद्वारे जोडलेले असतात समन्वय दुवा (साइड व्हॅलेन्सी) आणि आयनिक बंध (मुख्य व्हॅलेन्स). 0.1-0.2 लांबीचे रासायनिक आणि धातूचे बंध nmभौतिक बंधांचे ऊर्जा मूल्य लक्षणीयरीत्या ओलांडते आणि अगदी हायड्रोजन बंध (लांबी ०.२४-०.३२ nm), जे भौतिक आणि रासायनिक बंधांमध्ये मध्यवर्ती स्थान व्यापते. बाँड्सची ध्रुवीयता देखील रासायनिक रचना आणि युनिट्सच्या रचनेवर अवलंबून असते, जी द्विध्रुवीय क्षणाच्या मूल्यानुसार मोजली जाते μ ओ, शुल्काचे उत्पादन आणि शुल्कांमधील अंतर (टेबल 1.3), तसेच पॉलिमरमधील इंटरमॉलिक्युलर परस्परसंवादाच्या पातळीच्या समान. बंधनांच्या ध्रुवीयतेवर अवलंबून, पॉलिमर असू शकते ध्रुवीय आणि नॉन-ध्रुवीय . सर्व सेंद्रिय कार्बन-चेन अॅलिफॅटिक (ध्रुवीय नसलेल्या) पॉलिमरचा द्विध्रुवीय क्षण शून्याच्या जवळ आहे. मॅक्रोमोलेक्यूल्सच्या संरचनेवर अवलंबून, त्यांच्यामध्ये फैलाव, अभिमुखता आणि प्रेरक बंध दिसू शकतात. विखुरणारा जेव्हा इलेक्ट्रॉन केंद्रकाभोवती फिरतात तेव्हा अणूंमध्ये तात्काळ द्विध्रुव दिसल्यामुळे बंध निर्माण होतात. ध्रुवीय मॅक्रोमोलेक्यूल्स द्वारे दर्शविले जातात अभिमुखता (द्विध्रुव-द्विध्रुवीय) कनेक्शन. ध्रुवीय मॅक्रोमोलेक्यूल्सच्या द्विध्रुवांच्या क्षेत्रात, नॉनपोलर मॅक्रोमोलेक्यूल्सचे देखील ध्रुवीकरण केले जाऊ शकते. कायमस्वरूपी आणि प्रेरित द्विध्रुवांच्या दरम्यान, प्रेरण संप्रेषणे
इंटरमॉलिक्युलर परस्परसंवादकमी आण्विक वजनाच्या द्रवांमध्ये विरघळण्याची पॉलिमरची क्षमता, कमी तापमानात वर्तन, लवचिक आणि इतर गुणधर्म निर्धारित करते. त्याची पातळी मोजली जाते विद्राव्यता मापदंड - संमिश्र युनिटमधील अणूंच्या वैयक्तिक गटांच्या आकर्षण स्थिरांकांच्या बेरजेने पॉलिमर घनतेच्या उत्पादनाचे गुणोत्तर ते युनिटचे आण्विक वजन. यासाठी ते वापरतात एकसंध ऊर्जा घनता (kJ/mol), जे परस्परसंवादी मॅक्रोमोलेक्यूल्स किंवा अणूंचे गट एकमेकांपासून अमर्यादपणे मोठ्या अंतरावर काढून टाकण्याच्या कार्याच्या समतुल्य आहे. काचेच्या संक्रमण तापमानात टी एस इंटरमॉलिक्युलर परस्परसंवादाची ऊर्जा थर्मल मोशनच्या ऊर्जेपेक्षा जास्त होते आणि पॉलिमर आत जाते घन विट्रिफाइड अवस्था . सह पॉलिमर टसहखोलीच्या वरच्या तापमानाला म्हणतात प्लास्टिक , आणि खोलीच्या तपमानाच्या खाली आणि विद्राव्यता पॅरामीटर 14-19 आहे ( एम . J/m 3 ) 1/2 – elastomers (रबर्स).
पॉलिमरचे आण्विक वजन आणि त्याचे निर्धारण करण्याच्या पद्धती. आण्विक वस्तुमान वितरण आणि मॅक्रोमोलेक्यूल्सचा आकार. घटक घटकांच्या व्यवस्थेच्या संख्येनुसार आणि क्रमानुसार पॉलिमरचे वर्गीकरण.
आण्विक वस्तुमान(MM) पॉलिमरच्या संरचनेचे एक महत्त्वाचे वैशिष्ट्य आहे, यांत्रिक गुणधर्मांची पातळी निश्चित करणे आणि विशिष्ट गटाशी संबंधित आहे: ऑलिगोमर्स (थर्मोसेट्स) - 10 3 -10 4, क्रिस्टलीय थर्मोप्लास्टिक्स - 10 4 -5 . 10 4, आकारहीन थर्मोप्लास्टिक्स - 5 . 10 4 -2 . 10 5, रबर – 10 5 -10 6. पॉलिमरचा एमएम जितका कमी असेल तितका त्यांच्या वितळण्याची स्निग्धता कमी असेल आणि ते तयार होण्यास सोपे जाईल. यांत्रिक गुणधर्म कडक होणे (ऑलिगोमर्स) आणि क्रिस्टलिनिटी (पॉलिमाइड्स, पॉलिस्टर्स) किंवा काचेच्या स्थितीत संक्रमणाच्या डिग्रीद्वारे अधिक निर्धारित केले जातात. सर्वोच्च एमएम हे रबर्स आहेत ज्यांना मोल्ड करणे कठीण आहे, परंतु त्यांच्यापासून बनवलेल्या उत्पादनांमध्ये उच्च लवचिकता असते. मोठ्या मेगावॅटमुळे समान प्रमाणात पॉलिमरायझेशन होत नसल्यामुळे, मॅक्रोमोलेक्यूल्स आकारात भिन्न असतात. पॉलीडिस्पर्सिटी (पॉलिमॉलिक्युरिटी) पॉलिमरच्या भौतिक रसायनशास्त्रातील मूलभूत संकल्पनांपैकी एक आहे, आणि प्रकार आण्विक वजन वितरण (MWD) हा एक महत्त्वाचा सूचक आहे जो MM पेक्षा कमी नसलेल्या पॉलिमरच्या भौतिक आणि यांत्रिक गुणधर्मांवर परिणाम करतो.
MM हे सरासरी सांख्यिकीय मूल्य असल्याने, ते निर्धारित करण्याच्या विविध पद्धती भिन्न मूल्ये देतात. सह विरळ संख्या डायल्युट पॉलिमर सोल्युशनमधील मॅक्रोमोलेक्यूल्सची संख्या निश्चित करण्यावर पद्धती आधारित आहेत, उदाहरणार्थ, त्यांचे ऑस्मोटिक दाब मोजून, आणि सरासरी वस्तुमान - मॅक्रोमोलेक्यूल्सचे वस्तुमान निर्धारित करताना, उदाहरणार्थ, प्रकाश विखुरणे मोजून. सरासरी संख्या MM ( Mn ) केवळ पॉलिमर नमुन्याचे वस्तुमान त्यातील मॅक्रोमोलेक्यूल्सच्या संख्येने विभाजित करून प्राप्त केले जाते आणि वस्तुमान सरासरी MM: M w =M 1 w 1 +M 2 w 2 +…+M i w i , कुठे w १ , w 2 , वाय - अपूर्णांकांचे वस्तुमान अपूर्णांक; मी १ , मी 2 , एम आय - वस्तुमान-सरासरी MM अपूर्णांक. सरासरी चिकटपणा एमएम, जे वस्तुमान सरासरी एमएम पर्यंत पोहोचते, ते सौम्य द्रावणांच्या चिकटपणाद्वारे निर्धारित केले जाते. पॉलिमर म्हणतात monodisperse , जर त्यात मॅक्रोमोलेक्युल आकारांसह एक अपूर्णांक एकमेकांच्या अगदी जवळ असेल आणि त्यासाठी गुणोत्तर मेगावॅट/Mn =१.०२-१.०५. इतर प्रकरणांमध्ये, वस्तुमान सरासरी MM संख्या सरासरी MM पेक्षा जास्त आहे आणि त्यांचे गुणोत्तर ( मेगावॅट/Mn =2.0-5.0) हे पॉलिमरच्या पॉलीडिस्पर्सिटीचे मोजमाप आहे. आणखी मेगावॅट/Mn , MMR जितका विस्तीर्ण. पॉलिमर MWD वक्र वर, मूल्य Mn जास्तीत जास्त खाते, म्हणजे अपूर्णांकामध्ये ज्याचा पॉलिमर रचनेत वाटा सर्वात मोठा आहे, आणि मेगावॅट x-अक्षाच्या बाजूने उजवीकडे सरकले.
पॉलिमर मॅक्रोमोलेक्यूल्सचा मोठा आकार त्यांच्या संरचनेचे आणखी एक वैशिष्ट्य निर्धारित करतो. ते असू शकतात रेखीय किंवा फांदया (मुख्य साखळीच्या बाजूच्या फांद्यांसह किंवा तारेच्या आकारात). जवळ एमएम मूल्ये बनतात isomers . रेखीय आणि ब्रँच केलेले मॅक्रोमोलिक्युल्स असलेल्या पॉलिमरचे गुणधर्म मोठ्या प्रमाणात बदलतात. शाखा - मॅक्रोमोलेक्यूल्सच्या संरचनेचा अवांछित सूचक, त्यांची नियमितता कमी करणे आणि पॉलिमरचे क्रिस्टलायझेशन गुंतागुंतीचे करणे. रासायनिक बंधांद्वारे मॅक्रोमोलेक्यूल्सचे कनेक्शन तयार होण्यास कारणीभूत ठरते जाळीदार संरचना , पुढे पॉलिमरचे गुणधर्म बदलत आहेत. मॅक्रोमोलेक्यूल्सच्या संरचनेतील अशा फरकांनुसार (चित्र 1.1), पॉलिमर म्हणतात. रेखीय , फांदया आणि जाळी (शिवणे ).
नंतरच्या प्रकरणात, "मॅक्रोमोलेक्यूल" ची संकल्पना त्याचा अर्थ गमावते, कारण संपूर्ण क्रॉस-लिंक केलेला पॉलिमर नमुना एक विशाल रेणू बनतो. म्हणून, क्रॉस-लिंक केलेल्या पॉलिमरमध्ये, मॅक्रोमोलेक्यूल्सला जोडणाऱ्या रासायनिक बंध (नेटवर्क नोड्स) दरम्यान साखळी विभागाच्या MM चे सरासरी मूल्य निर्धारित केले जाते.
कॉपॉलिमरमुख्य साखळीमध्ये दोन किंवा अधिक वेगवेगळ्या मोनोमरची एकके असतात (उदाहरणार्थ, स्टायरीन-बुटाडियन रबर) आणि त्यापेक्षा अधिक जटिल रचना असते homopolymers , एका मोनोमरच्या युनिट्सचा समावेश होतो. मॅक्रोमोलेक्युलमधील मोनोमर युनिट्सच्या यादृच्छिक संयोजनासह कॉपॉलिमर म्हणतात. सांख्यिकीय , त्यांच्या योग्य बदलासह - पर्यायी , आणि एका मोनोमरच्या युनिट्सच्या मोठ्या प्रमाणात विभाग (ब्लॉक) सह - ब्लॉक कॉपॉलिमर . जर एका मोनोमरचे ब्लॉक्स मॅक्रोमोलेक्युलच्या मुख्य साखळीला जोडलेले असतील, तर दुसर्या मोनोमरच्या युनिट्सने बनलेले, मोठ्या बाजूच्या शाखांच्या रूपात, तर कॉपॉलिमर म्हणतात. लसीकरण केले . कॉपॉलिमरची रचना रासायनिक रचना आणि ब्लॉक्स किंवा ग्राफ्ट चेनची लांबी आणि मॅक्रोमोलेक्युलमधील ब्लॉक्स किंवा ग्राफ्ट्सच्या संख्येद्वारे दर्शविली जाते. समान किंवा भिन्न मोनोमर्सची युनिट्स जोडली जाऊ शकतात नियमितपणे (एकाचा शेवट - दुसर्याची सुरुवात) किंवा अनियमितपणे (एकाचा शेवट दुसर्याचा शेवट असतो, दुसर्याची सुरूवात ही तिसर्या दुव्याची सुरुवात असते, इ.) आणि बाजूच्या गटातील पर्यायांमध्ये नियमित किंवा अनियमित अवकाशीय व्यवस्था असू शकते. मॅक्रोमोलेक्यूलची रचना त्याच्या कॉन्फिगरेशन आणि कॉन्फॉर्मेशनद्वारे देखील निर्धारित केली जाते.
मॅक्रोमोलेक्यूल्स आणि स्टिरिओइसॉमर्सचे कॉन्फिगरेशन. मॅक्रोमोलेक्यूल्सची रचना आणि लवचिकता. लवचिक आणि कठोर साखळी पॉलिमर आणि त्यांच्या मॅक्रोमोलेक्यूल्सचा आकार.
मॅक्रोमोलेक्यूल कॉन्फिगरेशन- ही त्याच्या अणूंची एक विशिष्ट अवकाशीय व्यवस्था आहे, जी थर्मल हालचाली दरम्यान बदलत नाही, परिणामी त्याचे विविध प्रकार स्थिर आयसोमर आहेत. Cis isomers प्रत्येक पुनरावृत्ती युनिटमध्ये दुहेरी बाँडच्या वेगवेगळ्या बाजूंवर भिन्न घटकांच्या स्थानाद्वारे वैशिष्ट्यीकृत, आणि ट्रान्स आयसोमर्स - दुहेरी बाँडच्या एका बाजूला विविध घटकांची उपस्थिती. अशा आयसोमर्सचे उदाहरण म्हणजे NA आणि gutta-percha - नैसर्गिक polyisoprenes रासायनिक संरचनेत एकसारखे आहेत. गुट्टा-पेर्चा हे स्फटिक रचना असलेले प्लास्टिक आहे जे 50-70 डिग्री सेल्सिअस तापमानात वितळते आणि एनके हे +100 ते तापमान श्रेणीतील इलास्टोमर आहे. ओते -72 पर्यंत ओ C, कारण त्यांचे मॅक्रोमोलिक्युल वेगळे आहेत ओळखीचा कालावधी . IN cis-पोलीसोप्रीन (NC) मिथाइल गट एका दिशेकडे वळतात, एका घटक युनिटमधून होतात, जे 0.82 च्या बरोबरीचे असते. nm, आणि त्याच्या मध्ये ट्रान्स-इसोमर (गुट्टा-पर्चा) - ०.४८ नंतर nm:
cis- 1,4-पॉलीसोप्रीन (NC)
ट्रान्स-1.4-पॉलीसोप्रीन
macromolecules पासून ऑप्टिकल पॉलिमर असममित कार्बन अणूसह, प्राप्त करण्यासाठी विशेष संश्लेषण पद्धती वापरल्या जातात स्टिरिओरेग्युलर आयसोमर्स - isotactic (पर्यायी मॅक्रोमोलेक्युल प्लेनच्या एका बाजूला असतात) आणि सिंडिओटॅक्टिक (प्रतिनिधी विरुद्ध बाजूस आहेत):
ते गुणधर्मांमध्ये भिन्न आहेत अॅटॅक्टिक पर्यायांच्या अनियमित व्यवस्थेसह पॉलिमर. प्रतिस्थापकांच्या परस्पर तिरस्कारामुळे अंतराळात एकमेकांच्या तुलनेत त्यांचे विस्थापन होते आणि म्हणून सममितीचे विमान सर्पिलच्या रूपात वाकते. सर्पिलची रचना जैविक दृष्ट्या सक्रिय पॉलिमरचे वैशिष्ट्य देखील आहे (उदाहरणार्थ, डीएनएचे दुहेरी हेलिक्स). स्टिरिओइसॉमर्सच्या मॅक्रोमोलेक्यूल्सची रचना त्यांच्या संश्लेषणाच्या पद्धतींबद्दल माहितीचा वाहक आहे आणि प्रथिनांमध्ये, डीएनएच्या दुहेरी हेलीस त्यांच्या जैविक आनुवंशिकतेबद्दल प्रचंड माहिती देतात.
मॅक्रोमोलेक्यूल कॉन्फॉर्मेशन- ही अणूंची किंवा अणूंच्या गटांची अवकाशीय व्यवस्था आहे, जी थर्मल गतीच्या प्रभावाखाली त्यांच्यातील रासायनिक बंध नष्ट न करता बदलू शकते. मॅक्रोमोलेक्युलची मोठी लांबी, निश्चित रासायनिक बंधांभोवती त्याच्या भागांच्या फिरण्याच्या शक्यतेसह, निर्धारित करते रोटेशनल आयसोमेरिझम , भिन्न स्वरूपाच्या स्वरुपात व्यक्त. हायड्रोजनचे अणू एकमेकांच्या जितके जवळ असतील ( cis-स्थिती), त्यांचे प्रतिकर्षण जितके जास्त असेल आणि त्यानुसार, मॅक्रोमोलेक्यूलची संभाव्य ऊर्जा. ध्रुवीय घटकांद्वारे परस्परसंवाद वाढविला जातो, जसे की क्लोरीन अणू. IN ट्रान्स-आयसोमर्स, मॅक्रोमोलेक्युलची संभाव्य ऊर्जा कमी आहे, अणूंची व्यवस्था पेक्षा अधिक अनुकूल आहे cis- isomers. ऊर्जा रोटेशन अडथळा मॅक्रोमोलेक्यूलचे भाग जे ते बनवतात प्रतिबंधित , दोलनांची मालिका असलेली, मात करण्यास मदत करते थर्मल ऊर्जा चढउतार . साध्या कनेक्शनभोवती दोलन आणि हालचालींचा संच ठरतो वक्रता करण्यासाठी अंतराळातील मॅक्रोमोलेक्यूल्स, जे वेगवेगळ्या दिशेने जाऊ शकतात आणि कालांतराने बदलू शकतात. दुसऱ्या शब्दांत, मॅक्रोमोलेक्यूल आहे लवचिकता - थर्मल हालचाली किंवा बाह्य शक्तींच्या कृतीचा परिणाम म्हणून त्याचे स्वरूप बदलण्याची क्षमता. मोठ्या संख्येने अणूंसह, साखळी केवळ वाकू शकत नाही, परंतु अगदी कुरळे करणे खूप सैल मॅक्रोमोलेक्युलर कॉइल , ज्याचा आकार दर्शविला जाऊ शकतो मूळ त्याच्या टोकांमधील चौरस अंतर आणि त्यातील घटक लिंक्सची संख्या जाणून गणितीय पद्धतीने गणना करा. मॅक्रोमोलेक्यूल्सच्या साखळीच्या रचनेमुळे, एका अणू किंवा गटाच्या हालचालीमुळे इतरांच्या हालचाली होतात, परिणामी सुरवंट किंवा अळीच्या हालचालीसारखी हालचाल होते, ज्याला म्हणतात. reptational (चित्र 1.2). साखळीचा एक भाग जो संपूर्णपणे गतीच्या प्राथमिक कृतीमध्ये हलतो त्याला म्हणतात साखळी विभाग . थर्मोडायनामिक लवचिकता थर्मल मोशनच्या प्रभावाखाली साखळीचे स्वरूप बदलण्याची क्षमता दर्शवते आणि कडकपणा पॅरामीटर, थर्मोडायनामिक सेगमेंटची लांबी किंवा फ्लोरी लवचिकता पॅरामीटरद्वारे त्याचे मूल्यांकन केले जाऊ शकते. हे निर्देशक जितके कमी असतील तितकी मॅक्रोमोलेक्युल एका कॉन्फॉर्मेशनमधून दुसर्यामध्ये संक्रमण होण्याची शक्यता जास्त असेल (तक्ता 1.4). कडकपणा पॅरामीटर सौम्य पॉलिमर सोल्यूशनमध्ये वास्तविक आणि मुक्तपणे जोडलेल्या साखळ्यांच्या टोकांमधील रूट-मीन-चौरस अंतराच्या गुणोत्तराने अंदाज लावला जातो. थर्मोडायनामिक विभागाची लांबी A (कुहन सेगमेंट) लिंक्सचा एक क्रम दर्शवितो ज्यामध्ये प्रत्येक दुवा इतरांपेक्षा स्वतंत्रपणे वागतो आणि साखळीच्या टोकांमधील रूट-मीन-चौरस अंतराशी देखील संबंधित असतो. हे अत्यंत कठोर साखळ्यांसाठी मॅक्रोमोलेक्यूलच्या हायड्रोडायनामिक लांबीच्या आणि अत्यंत लवचिक साखळ्यांसाठी पुनरावृत्ती युनिटच्या लांबीइतके आहे. डायन मालिकेतील पॉलिमर आणि मुख्य साखळीतील ~Si-O~ किंवा ~C-O~ बॉण्ड्स हे विनाइल सिरीजच्या पॉलिमरच्या तुलनेत अधिक लवचिकतेने वैशिष्ट्यीकृत आहेत, कारण CH मधील विनिमय परस्परसंवाद कमी झाल्यामुळे 2 -गटांमध्ये रोटरी आयसोमर्सच्या 100 पट कमी ऊर्जा असते. घटकांच्या स्वरूपाचा मॅक्रोमोलेक्यूल्सच्या लवचिकतेवर थोडासा प्रभाव पडतो. फ्लोरी लवचिकता पॅरामीटर f ओमॅक्रोमोलेक्युलमध्ये लवचिक बंधांची सामग्री दर्शविते आणि लवचिकता निकष म्हणून काम करते ज्याद्वारे पॉलिमर विभागले जातात लवचिक साखळी (f ओ>0,63; ए<10nm) आणि कडक साखळी (f ओ<0,63; ए>35nm). नंतरचे मॅक्रोमोलेक्युलर कॉइलच्या रूपात नसतात आणि त्यांच्याकडे मॅक्रोमोलेक्यूल्सचा लांबलचक आकार असतो - एक लवचिक स्ट्रिंग (पॉलीलकाइल आयसोसायनेट, ए =100), क्रँकशाफ्ट (पॉली- पी- बेंझामाइड, ए =210) किंवा सर्पिल (बायोपॉलिमर, ए =240).गतीज लवचिकता मॅक्रोमोलेक्युल बल फील्डमधील त्याच्या संक्रमणाचा दर एका कॉन्फॉर्मेशनमधून दुसऱ्या कॉन्फॉर्मेशनमध्ये प्रतिबिंबित करतो आणि मूल्याद्वारे निर्धारित केला जातो गतिज विभाग , म्हणजे मॅक्रोमोलेक्यूलचा तो भाग जो संपूर्णपणे बाह्य प्रभावांना प्रतिसाद देतो. थर्मोडायनामिक विभागाच्या विपरीत, ते तापमान आणि बाह्य प्रभावाच्या गतीद्वारे निर्धारित केले जाते. वाढत्या तापमानासह, गतिज ऊर्जा आणि मॅक्रोमोलेक्युलची लवचिकता वाढते आणि गतिज विभागाचा आकार कमी होतो. ज्या परिस्थितीत बलाच्या क्रियेचा काळ एका रूपांतरातून दुसर्या रूपांतरात संक्रमण होण्याच्या वेळेपेक्षा जास्त असतो, गतीज लवचिकता जास्त असते आणि गतिज विभाग परिमाणात थर्मोडायनामिक विभागाकडे जातो. वेगवान विकृती दरम्यान, गतिज विभाग हा मॅक्रोमोलेक्यूलच्या हायड्रोडायनामिक लांबीच्या जवळ असतो आणि थर्मोडायनामिकली लवचिक साखळी देखील कठोर प्रमाणे वागते. पृथक मॅक्रोमोलेक्युलची गतीशील लवचिकता अत्यंत सौम्य द्रावणांच्या व्हिस्कोइलास्टिक गुणधर्मांवरून निर्धारित केली जाते आणि त्यानंतरच्या एक्स्ट्रापोलेशन ते शून्य एकाग्रतेवर होते. लवचिक-साखळी अनाकार पॉलिमरच्या मॅक्रोमोलेक्यूल्समध्ये असतात चेंडूच्या आकाराचे दोन्ही वेगळ्या स्वरूपात आणि मोठ्या प्रमाणात. शिवाय, पॉलिमरची रचना "मॉलेक्युलर फील" च्या संरचनेसारखी नाही, ज्यामध्ये मॅक्रोमोलिक्युल्स अव्यवस्थितपणे अडकलेले असतात, जसे पूर्वी विचार केला गेला. अनाकार पॉलिमरमध्ये क्रमबद्ध प्रदेशांची कल्पना 1948 मध्ये अल्फ्रेने व्यक्त केली होती.
मॅक्रोमोलेक्यूल कॉन्फिगरेशन अन्यथाप्राथमिक रचना(इंग्रजी) - मध्ये अणूंची अवकाशीय व्यवस्था बाँड कोनांची मूल्ये आणि संबंधित बाँडच्या लांबीद्वारे निर्धारित केले जाते.
वर्णन
मॅक्रोमोलेक्यूलचे कॉन्फिगरेशन त्याच्या घटक मोनोमर युनिट्सच्या सापेक्ष स्थितीद्वारे तसेच त्यांच्या संरचनेद्वारे निर्धारित केले जाते. सध्या, "संरचना" किंवा "प्राथमिक संरचना" हा शब्द सामान्यतः मॅक्रोमोलेक्यूल्सच्या कॉन्फिगरेशनचे वर्णन करण्यासाठी वापरला जातो.
शॉर्ट-रेंज (शेजारच्या युनिट्सच्या संलग्नकांचे कॉन्फिगरेशन) आणि लांब-श्रेणी कॉन्फिगरेशन ऑर्डरमध्ये फरक केला जातो, जो मॅक्रोमोलेक्यूल्सच्या बर्यापैकी विस्तारित विभागांची रचना दर्शवतो. चातुर्य (ऑर्डर) चे परिमाणात्मक माप म्हणजे स्टिरिओरेग्युलरिटीची डिग्री. याव्यतिरिक्त, विविध प्रकारच्या जवळच्या शेजारी जोड्यांच्या संख्येद्वारे युक्तीचे वर्णन केले जाऊ शकते (di-, tri-, tetrad), ज्याचे वितरण प्रायोगिकरित्या निर्धारित केले जाते. सांख्यिकीय नेटवर्क मॅक्रोमोलेक्यूल्सच्या कॉन्फिगरेशनचे एक परिमाणात्मक वैशिष्ट्य, उदाहरणार्थ, क्रॉस-लिंकिंग घनता, म्हणजे, नेटवर्क नोड्समधील साखळीचा सरासरी विभाग.
मॅक्रोमोलेक्यूल्सचे कॉन्फिगरेशन एक्स-रे डिफ्रॅक्शन विश्लेषण, बायरफ्रिंगन्स इत्यादीद्वारे निर्धारित केले जाते. नियमानुसार, प्रत्येक पद्धत कोणत्याही कॉन्फिगरेशन वैशिष्ट्यासाठी सर्वात "संवेदनशील" असते; अशाप्रकारे, एनएमआर अनेक प्रकरणांमध्ये कमी-श्रेणीच्या कॉन्फिगरेशन ऑर्डरचे परिमाणात्मक वर्णन करणे शक्य करते.
· सेंद्रिय पॉलिमर(रचनेत ऑर्गोजेनिक घटकांचा समावेश होतो - C, N, O, P, S) ते होमोचेन (मुख्य साखळीमध्ये फक्त कार्बन अणू असतात) आणि हेटरोचेन (मुख्य साखळीत इतर अणूंचा समावेश असतो) मध्ये विभागले जातात. पॉलिमरच्या या वर्गात बायोपॉलिमरचा समावेश होतो.
· ऑर्गेनोएलिमेंट पॉलिमर(मुख्य साखळीमध्ये, कार्बन अणूंसह, Si, Al, Ti, Ge, B चे अणू आहेत).
· अजैविक पॉलिमर (मुख्य साखळीमध्ये कार्बन अणू नसतात, जसे की सिलिकॉन).
1. पॉलिमर नामांकनाच्या प्रकारांची यादी करा.
2. मोनोमर्सच्या नावांवर आधारित नामांकन कसे तयार केले जाते?
3. पॉलिमर साखळीच्या रासायनिक संरचनेवर आधारित नामांकन वापरून पॉलिमर नावांची उदाहरणे द्या.
4. पॉलिमरच्या वर्गीकरणाच्या प्रकारांची नावे सांगा. उदाहरणे द्या.
5. कॉपॉलिमरचे कोणते प्रकार आहेत?
6. पॉलिमरचे रासायनिक वर्गीकरण कसे केले जाते?
स्वतंत्र निराकरणासाठी समस्या*
2. मुख्य पॉलिमरचे वर्गीकरण आणि संरचनात्मक सूत्रे
2.1 पॉलिमरचे वर्गीकरण
प्रश्न 2501 - 2502, 2403 - 2406, 2307
२.२. मुख्य पॉलिमरची संरचनात्मक सूत्रे
प्रश्न ३५०१, ३४०२, ३३०३ – ३३०९
*येथे आणि पुढील मध्ये, "केमिस्ट्री अँड फिजिक्स ऑफ पॉलिमर", M., MITHT, 2009 या विषयातील "थीमॅटिक आणि अंतिम नियंत्रणासाठी चाचणी कार्यांचे संकलन" मधून कार्ये दिली आहेत.
कलम 3. मॅक्रोमोलेक्यूल्सची मुख्य वैशिष्ट्ये
मॅक्रोमोलेक्यूल्स 4 मुख्य पॅरामीटर्सद्वारे दर्शविले जातात:
1. आण्विक वजन (MM), आण्विक वस्तुमान वितरण (MWD);
2. मॅक्रोमोलेक्यूल कॉन्फिगरेशन;
3. मॅक्रोमोलेक्यूलची रचना;
4. टोपोलॉजी (रेखीय, शाखायुक्त).
· MM तुम्हाला मॅक्रोमोलिक्युल्सची लांबी आणि आकार निर्धारित करण्यास अनुमती देते;
· कॉन्फिगरेशन मॅक्रोमोलेक्यूल्सची रासायनिक रचना ठरवते;
· कॉन्फॉर्मेशन मॅक्रोमोलेक्यूल्सचा आकार ठरवते.
३.१. आण्विक वजन (MM), आण्विक वजन वितरण (MWD)
IUD आणि NMS साठी MM च्या संकल्पनेतील मुख्य फरक:
MW हे रेषीय पॉलिमरसाठी आण्विक लांबीचे मोजमाप आहे आणि कमी आण्विक वजन घटक पुनरावृत्ती युनिट्सच्या MW च्या संदर्भात व्यक्त केले जाऊ शकते:
https://pandia.ru/text/78/135/images/image040_18.gif" width="12" height="2 src=">m0 – कंपाऊंड रिपीटिंग युनिटचे आण्विक वजन;
पीएन - पॉलिमरायझेशनची डिग्री
बहुतेक सिंथेटिक पॉलिमर वैयक्तिक संयुगे नसतात, परंतु वेगवेगळ्या आकाराच्या परंतु समान रचना असलेल्या रेणूंचे मिश्रण असतात.
हे ठरते:
पॉलिमरसाठी, पॉलीडिस्पर्सिटीमुळे प्रभावी आण्विक वजन सरासरी मूल्य आहे - आण्विक वजनामध्ये मॅक्रोमोलेक्यूल्सचा प्रसार;
· बहुतेक पॉलिमरसाठी, शेवटचे गट पॉलिमर साखळीतील लिंक्सच्या रचनेपेक्षा वेगळे असतात;
· मॅक्रोमोलेक्यूल्समध्ये काही बाजूच्या शाखा असू शकतात, यामुळे मॅक्रोमोलेक्यूल्स देखील एकमेकांपासून वेगळे होतात;
· बहुतेक बायोपॉलिमर वैयक्तिक संयुगे असतात (प्रत्येक विशिष्ट पॉलिमर रचना, रचना आणि आण्विक वजनात अद्वितीय असतो).
पॉलीडिस्पर्सिटीची कारणे:
1. पॉलिमर उत्पादन प्रक्रियेच्या सांख्यिकीय स्वरूपामुळे: संश्लेषण प्रक्रियेदरम्यान, विविध लांबीचे मॅक्रोमोलेक्यूल्स प्राप्त होतात;
2. मॅक्रोमोलेक्यूल्सच्या आंशिक विनाशाच्या प्रक्रियेमुळे, उदाहरणार्थ, सामग्रीच्या ऑपरेशन दरम्यान;
3. पॉलिमर रेणूच्या शेवटच्या गटांमधील फरकामुळे;
4. काही पॉलिमरच्या वेगवेगळ्या ठिकाणी शाखा आणि वेगवेगळ्या रासायनिक रचना असल्याच्या वस्तुस्थितीमुळे.
3.1.1. आण्विक वस्तुमानांची सरासरी काढण्याच्या पद्धती
1) रेणूंच्या संख्येपेक्षा सरासरी
संख्या सरासरी MM:
Мw=∑(Ni Mi2)/∑(NiMi) (3.1.1.2)
दिलेल्या आण्विक वजनाच्या अंशाचे वस्तुमान विचारात घेतले जाते.
Mw क्रोमॅटोग्राफी, अल्ट्रासेंट्रीफ्यूगेशन आणि लाइट स्कॅटरिंग पद्धती वापरून निर्धारित केले जाते.
Kn=Mw/Mn (3.1.1.3)
मोनोडिस्पर्स (जैविक) पॉलिमर Kn=1 साठी.
एका अरुंद वितरणासह Kn=1.01÷1.05.
उद्योगात, Kn=3÷10 सह पॉलिमर बहुतेकदा तयार केले जातात.
3) सरासरी स्निग्धता मिमी:
Mŋ=((∑NiMi)1+α/∑(NiMi))1/α, 0<α<1 (3.1.1.4)
![]()
३.१.२. आण्विक वस्तुमान वितरण (MWD)
पॉलिमरच्या आण्विक वजनाचे सर्वात संपूर्ण वैशिष्ट्य म्हणजे आण्विक वजन वितरण कार्य.
नायट्रोजन, बोरॉन आणि अॅल्युमिनियम हे पॉलिमर संरचनेच्या इतर घटकांमधील मॅक्रोमोलेक्युलर चेनचे घटक असू शकतात किंवा मुख्य शृंखलामध्ये हेटरोएटम्स म्हणून समाविष्ट केले जाऊ शकतात.

४.३. कार्बन
त्याच्या स्वतःच्या अणूंमध्ये आणि इतर अणूंसह मजबूत सहसंयोजक बंध तयार करण्याची प्रवृत्ती जास्त आहे.
https://pandia.ru/text/78/135/images/image064_12.gif" width="102" height="92"> - ग्राफीन, ग्रेफाइट आणि काजळीची द्विमितीय कार्बन-कार्बन रचना
कार्बन अणूंची रेखीय साखळी मिळवणे देखील शक्य आहे:
https://pandia.ru/text/78/135/images/image066_10.gif" width="238" height="14 src=">
गरम झाल्यावर ते ग्रेफाइटमध्ये बदलते.
जेव्हा कार्बनचे 1 किंवा 2 व्हॅलेन्स इतर अणू किंवा गटांसह संतृप्त होतात तेव्हा कार्बन अणूंपासून रेखीय मॅक्रोमोलिक्यूल्स तयार करण्याच्या खूप मोठ्या संधी उघडतात.
 - पॉलिथिलीन
- पॉलिथिलीन
 - पॉलीप्रोपीलीन
- पॉलीप्रोपीलीन
![]() - पॉलिटेट्राफ्लुरोइथिलीन
- पॉलिटेट्राफ्लुरोइथिलीन
तसेच, मुख्य साखळीमध्ये हेटरोएटम्स असलेले विविध गट असू शकतात:
https://pandia.ru/text/78/135/images/image071_11.gif" width="93" height="43 src="> - एस्टर गट
https://pandia.ru/text/78/135/images/image073_9.gif" width="105" height="45 src="> - कार्बामाइड (युरिया) गट
https://pandia.ru/text/78/135/images/image076_9.gif" width="185 height=84" height="84">
परंतु ते फारसे रासायनिकदृष्ट्या स्थिर नसतात आणि ऑक्सिडेशन दरम्यान, सिलिकॉन ऑक्सिजनशी बांधले जातात, खूप मजबूत सिलिकॉन-ऑक्सिजन बंध तयार करतात.
निसर्गात, सिलिकॉन क्वार्ट्जच्या स्वरूपात आढळते:

ही एक कठोर त्रिमितीय रचना आहे जी रेखीय मॅक्रोमोलेक्यूल्सचे "पॉलिमरिक" गुणधर्म प्रदर्शित करत नाही. रेखीय मॅक्रोमोलेक्यूल्स प्रत्येक सिलिकॉन अणूच्या दोन व्हॅलेन्सीजला सेंद्रिय रॅडिकल्स (CH3-, C2H5-, इ.) सह बदलून प्राप्त केले जातात. या प्रकरणात, सिलिकॉन-ऑर्गेनिक पॉलिमर दिसतात.
सिलिकॉन असलेले पॉलिमर संश्लेषित केले जाऊ शकतात:
 - पॉलीसिलॉक्सेन
- पॉलीसिलॉक्सेन
Al, B, Ti, Zn आणि इतर काही अणू साखळीत बांधले जाऊ शकतात.
४.५. फॉस्फरस
फॉस्फरसचे अणू पॉलिमर बनवू शकतात, परंतु मुख्य साखळीमध्ये इतर अणू (बहुतेकदा ऑक्सिजन) समाविष्ट करणे आवश्यक आहे:
 - पॉलीफॉस्फेट्स
- पॉलीफॉस्फेट्स
 - पॉलीफॉस्फोरिक ऍसिड
- पॉलीफॉस्फोरिक ऍसिड
ऑर्थोफॉस्फोरिक ऍसिडचे अवशेष नैसर्गिक पॉलिमरमध्ये आढळतात (न्यूक्लिक ऍसिड, डीएनए आणि आरएनए):

अशा प्रकारे, द्विसंयोजक किंवा बहुसंयोजक अणू (C, O, P, N, S, Si, Al, B आणि काही इतर) मॅक्रोमोलिक्यूल्सच्या मुख्य शृंखलाच्या घटकांच्या रूपात किंवा बाजूच्या तुकड्यांमध्ये स्थित असू शकतात; मोनोव्हॅलेंट अणू (H, F, Cl, J, Br आणि काही इतर) केवळ पर्याय म्हणून मांडले जाऊ शकतात.
पॉलिमर रसायनशास्त्र या घटकांच्या आधारे तयार केले जाते.
४.६. पॉलिमरचे प्रकार
पॉलिमर एकतर कृत्रिमरित्या मिळवले जातात किंवा सजीवांपासून (बायोपॉलिमर) काढले जातात किंवा आधीच वेगळ्या नैसर्गिक पॉलिमरवर प्रक्रिया करून.
काही कृत्रिमरित्या तयार केलेले पॉलिमर निसर्गात अस्तित्वात आहेत. पॉलिमर मोनोमर्सपासून प्राप्त केले जातात - कमी-आण्विक पदार्थ किंवा तयार पॉलिमर (सिंथेटिक किंवा नैसर्गिक) च्या परिवर्तनाचा परिणाम म्हणून - पॉलिमर-सदृश परिवर्तन.

1,4-cis-polybutadiene निसर्गात अस्तित्वात नाही; ते कृत्रिमरित्या बुटाडीनपासून मिळते.

1,4-cis-polyisoprene निसर्गात अस्तित्वात आहे (नैसर्गिक रबर), परंतु निसर्गात ग्लुकोज आणि इतर पदार्थांपासून संश्लेषित केले जाते (परंतु उद्योगाप्रमाणे आयसोप्रीनपासून नाही)

हे पॉलिस्टर पॉली-बीटा-हायड्रॉक्सीब्युटायरेटच्या संक्षेपाने मिळू शकते आणि त्याच वेळी ते अनेक जीवाणूंद्वारे संश्लेषित देखील केले जाते.
या कोर्समध्ये बायोपॉलिमरचे संश्लेषण विचारात घेतले जाणार नाही.
अनेक नैसर्गिक पॉलिमर कृत्रिमरित्या तयार करणे खूप कठीण आहे. जटिल जैवरासायनिक प्रतिक्रियांच्या परिणामी ते सजीवांमध्ये तयार होतात.
सर्वात महत्वाचे नैसर्गिक पॉलिमर:
उदाहरणांमध्ये प्रतिक्रियांचा समावेश आहे पॉलिस्टरिफिकेशन:
HO-R-COOH + HO-R-COOH > HO-R-COO-R-COOH + H2O, इ.
polyamidation:
H2N-R-NH2 + ClOC-R"-COCl > H2N-R-NHCO-R"-COCl + HCl, इ.
शिवाय, पॉलिमरायझेशनच्या विपरीत, या प्रकरणात पॉलीकॉन्डेन्सेशन उत्पादनांची मूलभूत रचना मोनोमर यौगिकांच्या रचनेशी जुळत नाही, कारण पॉलीकॉन्डेन्सेशनची प्रत्येक रासायनिक क्रिया कमी आण्विक वजनाच्या उत्पादनाच्या रेणूच्या प्रकाशनासह असते.
पॉलीकॉन्डेन्सेशनची वरील सामान्य योजना काही प्रकारच्या प्रक्रियांशी सुसंगत आहे ज्या कमी आण्विक वजन उत्पादनांच्या प्रकाशनासह नसतात. यामध्ये, उदाहरणार्थ, ग्लायकोल आणि डायसोसायनेट्सपासून पॉलीयुरेथेनचे संश्लेषण समाविष्ट आहे:
HO-R-OH + O=C=N-R"-N=C=O > HO-R-O-CO-NH-R"-N=C=O, इ.
अशा polycondensation प्रक्रिया अनेकदा म्हणतात पॉलीअॅडिशन. गतिज नियमांनुसार, पॉलीअॅडिशन रिअॅक्शन या पॉलीकॉन्डेन्सेशन रिअॅक्शन्ससारख्याच असतात. दोन्ही प्रकारच्या पॉलीकॉन्डेन्सेशन प्रक्रियेमध्ये, मॅक्रोमोलेक्यूल्सची वाढ मोनोमर रेणूंच्या कार्यात्मक गटांच्या परस्परसंवादाद्वारे किंवा वेगवेगळ्या आण्विक वजनांच्या आधीच तयार केलेल्या साखळींच्या टोकांवर स्थित समान गटांच्या परस्परसंवादाद्वारे केली जाते. या प्रतिक्रियांच्या परिणामी प्राप्त होणारी इंटरमीडिएट पॉलिमर उत्पादने बर्यापैकी स्थिर असतात आणि ते मुक्त स्वरूपात वेगळे केले जाऊ शकतात. तथापि, त्यांच्या टोकांना प्रतिक्रियाशील गट असतात आणि म्हणून ते एकमेकांशी आणि संबंधित मोनोमर रेणूंसह पुढील संक्षेपण प्रतिक्रिया करण्यास सक्षम असतात. हे खालीलप्रमाणे आहे की सैद्धांतिकदृष्ट्या, पॉलीकॉन्डेन्सेशन केवळ तेव्हाच पूर्ण मानले जाऊ शकते जेव्हा सर्व टर्मिनल कार्यात्मक गट प्रतिक्रिया देतात, परिणामी एक विशाल चक्रीय मॅक्रोमोलेक्युल तयार होतो. व्यवहारात मात्र हे कधीच साध्य होत नाही.
स्वतंत्र अभ्यासासाठी प्रश्नः
1. आवर्त सारणीतील कोणते घटक पॉलिमर साखळी तयार करण्यास सक्षम आहेत?
2. सिंथेटिक पद्धतीने तयार केलेल्या पॉलिमरची उदाहरणे द्या.
3. नैसर्गिक पॉलिमरची उदाहरणे द्या.
4. पॉलिमरायझेशन प्रतिक्रियामध्ये कोणते मोनोमर्स भाग घेऊ शकतात?
१.३. मॅक्रोमोलेक्यूल्सचे कॉन्फिगरेशन
कॉन्फिगरेशनच्या संकल्पनेमध्ये मॅक्रोमोलेक्यूल्सच्या अणूंची विशिष्ट स्थानिक व्यवस्था समाविष्ट आहे, जी थर्मल हालचाली दरम्यान बदलत नाही. रासायनिक बंध तोडल्याशिवाय एका कॉन्फिगरेशनमधून दुसर्या कॉन्फिगरेशनमध्ये संक्रमण अशक्य आहे.
आहेत: 1) लिंक कॉन्फिगरेशन, 2) शॉर्ट-रेंज ऑर्डर - कनेक्टिंग लिंक्सचे कॉन्फिगरेशन, 3) लाँग-रेंज ऑर्डर - मोठ्या विभागांचे कॉन्फिगरेशन (उदाहरणार्थ, ब्लॉक्स आणि त्यांचे पर्याय, किंवा शाखांची लांबी आणि वितरण) , 5) संपूर्णपणे वाढवलेल्या साखळीचे कॉन्फिगरेशन.
लिंक कॉन्फिगरेशन. डायन पॉलिमरची सीआयएस आणि ट्रान्स कॉन्फिगरेशन ही उदाहरणे आहेत
1,4-cis-polyisoprene 1,4-trans-polyisoprene (नैसर्गिक रबर) (gutta-percha) दुसरे उदाहरण म्हणजे l,d-isomerism. उदाहरणार्थ,
~CH2 –CHR~ युनिट्स असलेल्या पॉलिमरसाठी, जेथे R कोणतेही मूलगामी आहे, तेथे दोन आयसोमर्सची निर्मिती शक्य आहे: l – levorotatory, आणि d – dextrorotatory
लिंक कनेक्शन कॉन्फिगरेशन(शॉर्ट रेंज ऑर्डर). साखळीतील दुवे “हेड टू टेल” किंवा “हेड टू हेड” प्रकार वापरून कनेक्ट केले जाऊ शकतात:

हेड-टू-टेल कनेक्शन आहे आणि हेड-टू-हेड कनेक्शनसाठी मोठ्या सक्रियता अडथळ्यांवर मात करणे आवश्यक आहे.
कॉपॉलिमरसाठी, होमोपॉलिमरच्या तुलनेत स्ट्रक्चरल आयसोमर्सचे प्रकार वाढतात. उदाहरणार्थ, बुटाडीन आणि स्टायरीनच्या कॉपॉलिमरसाठी हे शक्य आहे:
1. लिंक्सचे अनुक्रमिक फेरबदल –A–B–A–B–A–B–,
2. डायड्स आणि ट्रायड्सच्या स्वरूपात लिंक्सचे संयोजन–AA–BBV–AA–BBV– ,
3. दुव्यांचे सांख्यिकीय संयोजन–AA–B–AA–BBB–A–B– . लांब श्रेणी कॉन्फिगरेशन ऑर्डरवर पसरते
मुख्य साखळीतील दहापट आणि शेकडो अणू. उदाहरणार्थ, ब्लॉक कॉपॉलिमरमधील ब्लॉक्सचे मोठे अनुक्रम किंवा समान स्टिरिओरेग्युलॅरिटी असलेल्या युनिट्सचे मोठे अनुक्रम (उदाहरणार्थ, आयसोटॅक्टिक, अटॅक्टिक आणि सिंडिओटॅक्टिक संरचना असलेले पॉलिमर).
आयसोटॅक्टिक अॅटॅक्टिक सिंडिओटॅक्टिक
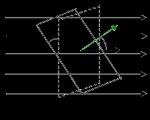
एकूण सर्किट कॉन्फिगरेशनलिंक्सच्या मोठ्या अनुक्रमांच्या परस्पर व्यवस्थेद्वारे निर्धारित केले जाते (लांब-श्रेणीच्या ऑर्डरसह). उदाहरणार्थ, ब्रँच केलेल्या मॅक्रोमोलेक्यूल्ससाठी, विविध प्रकारचे कॉन्फिगरेशन आकृती 4 मध्ये दर्शविले आहे.
तांदूळ. 4. मॅक्रोमोलेक्यूल्सचे कॉन्फिगरेशन

१.४. मॅक्रोमोलेक्यूल्सची रचना
कॉन्फॉर्मेशन हे अणूंच्या जागेत किंवा मॅक्रोमोलेक्युल बनवणार्या अणूंच्या गटातील एक परिवर्तनीय वितरण आहे. थर्मल मोशन किंवा बाह्य शक्तींच्या प्रभावाखाली एकल बंधांभोवती एककांच्या रोटेशन, रोटेशन किंवा कंपनामुळे एका संरचनेतून दुस-यामध्ये संक्रमण होऊ शकते आणि रासायनिक बंध तुटण्यासोबत नाही.
पॉलिमर भिन्न रूपे घेऊ शकतात:
सांख्यिकीय चेंडूदुमडलेली रचना आहे. जेव्हा अंतर्गत थर्मल हालचालीची तीव्रता बाह्य प्रभावापेक्षा जास्त असते तेव्हा तयार होते. रेखीय पॉलिमरचे वैशिष्ट्य [PE, PP, PB, PIB आणि शिडी पॉलिमर (पॉलीफेनिलिन सिलोक्सेन).
हेलिक्स - एच-बॉन्ड्समुळे पॉलिमरमध्ये तयार होतो (उदाहरणार्थ, प्रथिने रेणू आणि न्यूक्लिक अॅसिडमध्ये).
ग्लोब्यूल हा गोलाकाराच्या जवळ असलेला आकाराचा एक अतिशय संक्षिप्त कण आहे. मजबूत इंट्रामोलेक्युलर परस्परसंवादासह पॉलिमरचे वैशिष्ट्य (उदाहरणार्थ, PTFE).
अल्काइल पॉलीसोसायनेट्समध्ये रॉड किंवा स्ट्रिंग आढळते.
पट रचना. क्रिस्टलीय स्थितीत पॉलिमरचे वैशिष्ट्य (उदाहरणार्थ, पीई).
क्रँकशाफ्ट कॉन्फॉर्मेशनपॉली-एन-बेंजेनामाइडमध्ये जाणवते.
अंजीर.5. मॅक्रोमोलेक्यूल्सची रचना
1.5. मॅक्रोमोलेक्यूल्सची लवचिकता
पॉलिमरचे अत्यंत लवचिक, विश्रांती आणि थर्मोमेकॅनिकल गुणधर्म तसेच त्यांच्या सोल्यूशनचे गुणधर्म निर्धारित करणे, लवचिकता ही पॉलिमरची सर्वात महत्वाची वैशिष्ट्ये आहे. लवचिकता हे दुव्यांचे थर्मल हालचाल किंवा बाह्य यांत्रिक प्रभावांच्या प्रभावाखाली मॅक्रोमोलेक्यूल्सचे आकार बदलण्याची क्षमता दर्शवते. लवचिकता हे एकमेकांच्या सापेक्ष दुवे किंवा मॅक्रोमोलेक्यूल्सच्या भागांच्या अंतर्गत रोटेशनमुळे होते. सर्वात सोप्या सेंद्रिय संयुगाचे उदाहरण वापरून रेणूंमधील अंतर्गत रोटेशनच्या घटनेचा विचार करूया - इथेन रेणू.
इथेन रेणू (CH3 –CH3) मध्ये, कार्बन अणू हायड्रोजन अणूंशी आणि सहसंयोजक (σ-बंध) द्वारे एकमेकांशी जोडलेले असतात आणि σ-बंध (बंध कोन) च्या दिशांमधील कोन 1090 28/ आहे. यामुळे इथेन रेणूमध्ये अंतराळात पर्यायी घटकांची (हायड्रोजन अणू) टेट्राहेड्रल व्यवस्था होते. इथेन रेणूमधील थर्मल मोशनमुळे, एक CH3 गट C-C अक्षाभोवती दुस-याच्या तुलनेत फिरतो. या प्रकरणात, अणूंची अवकाशीय व्यवस्था आणि रेणूची संभाव्य ऊर्जा सतत बदलत असते. ग्राफिकदृष्ट्या, रेणूमधील अणूंच्या विविध टोकाच्या मांडणी रेणूच्या क्षैतिज समतल (चित्र 6) वरच्या प्रक्षेपणाच्या रूपात दर्शवल्या जाऊ शकतात. आपण असे गृहीत धरू या की स्थिती a मध्ये रेणूची संभाव्य ऊर्जा U1 च्या बरोबरीची आहे, आणि स्थिती b – U2 मध्ये, तर U1 ≠ U2, म्हणजे. रेणूचे स्थान ऊर्जावान असमान आहेत. स्थिती b, ज्यामध्ये H अणू एकमेकांच्या खाली स्थित आहेत, ते ऊर्जादृष्ट्या प्रतिकूल आहे, कारण H अणूंमध्ये प्रतिकारक शक्ती दिसतात, जे अणूंना ऊर्जावान अनुकूल स्थितीत स्थानांतरित करतात a. आम्ही स्वीकारल्यास
U1 =0, नंतर U2 = कमाल.

तांदूळ. 6. इथेन रेणूमधील अंतराळातील H अणूंच्या अत्यंत स्थानांसाठी प्रोजेक्शन सूत्रे.
तांदूळ. 7. मिथाइल समूहाच्या रोटेशनच्या कोनावर रेणूच्या संभाव्य ऊर्जेचे अवलंबन.
जेव्हा एक CH3 गट दुसर्याच्या सापेक्ष 600 ने फिरतो, तेव्हा रेणू a स्थानावरून b वर जातो आणि नंतर 600 नंतर पुन्हा a स्थानावर जातो, इ. रोटेशन कोन φ वर अवलंबून इथेन रेणूच्या संभाव्य उर्जेतील बदल अंजीर 7 मध्ये दर्शविला आहे. कमी सममिती असलेल्या रेणूंचा (उदाहरणार्थ, डायक्लोरोइथेन रेणू) अधिक जटिल संबंध U=f(φ) असतो.
संभाव्य (U 0 ) किंवा सक्रियकरण अडथळा रोटेशन
tion ही किमान स्थितीपासून कमाल संभाव्य ऊर्जेच्या स्थितीत रेणूच्या संक्रमणासाठी आवश्यक ऊर्जा आहे. इथेनसाठी, U0 लहान आहे (U0 = 11.7 kJ/mol) आणि at
सामान्य तापमानात, CH3 गट उच्च वेगाने (1010 rpm) C-C बाँडभोवती फिरतात.
जर रेणूमध्ये U0 पेक्षा कमी उर्जा राखीव असेल तर तेथे कोणतेही रोटेशन नाही आणि किमान उर्जेच्या स्थितीच्या सापेक्ष अणूंचे फक्त कंपन होते - हे मर्यादित आहे किंवा
मंद रोटेशन.
पॉलिमरमध्ये, इंट्रा- आणि इंटरमॉलिक्युलर परस्परसंवादामुळे, अवलंबित्व U=f(φ) एक जटिल आकार आहे.
जर साखळी दुव्याची एक स्थिती संभाव्य उर्जा U1 आणि दुसरी U2 द्वारे दर्शविली असेल, तर एका स्थानावरून दुसर्या स्थानावर संक्रमणाची ऊर्जा ∆U= U1 – U2 या फरकाच्या बरोबरीची आहे. मॅक्रोमोलेक्युल युनिटच्या एका समतोल स्थितीपासून दुस-या स्थानापर्यंत संक्रमण ऊर्जा ∆U मध्ये फरक दर्शवतो थर्मोडायनामिक लवचिकता. हे थर्मल हालचालींच्या प्रभावाखाली वाकण्याची साखळीची क्षमता निर्धारित करते.
लवचिकतेचे आणखी एक वैशिष्ट्य म्हणजे दुव्यांचे एका स्थानावरून दुस-या स्थानावर संक्रमणाची गती. संरचनात्मक परिवर्तनाचा दर U0 च्या मूल्याच्या गुणोत्तरावर आणि बाह्य प्रभावांच्या ऊर्जेवर अवलंबून असतो. U0 जितका मोठा असेल तितकी लिंक्स वळतात आणि कमी लवचिकता. U0 मूल्याद्वारे निर्धारित केलेल्या मॅक्रोमोलेक्यूल्सची लवचिकता म्हणतात गतिज लवचिक
मॅक्रोमोलेक्यूल्सची लवचिकता निर्धारित करणारे घटक
अशा घटकांमध्ये हे समाविष्ट आहे: U0 चे मूल्य, पॉलिमरचे आण्विक वस्तुमान, अवकाशीय नेटवर्कची घनता, घटकांचा आकार आणि तापमान.
संभाव्य रोटेशन अडथळा (U 0). U0 चे मूल्य इंट्रा- आणि इंटरमॉलिक्युलर परस्परसंवादावर अवलंबून असते. कार्बन-चेन पॉलिमरमधील U0 आणि साखळी लवचिकता प्रभावित करणाऱ्या घटकांचा विचार करूया.
कार्बन चेन पॉलिमर
कार्बन-चेन पॉलिमरमध्ये, सर्वात कमी ध्रुवीय संतृप्त हायड्रोकार्बन्स असतात. त्यांचे इंट्रा- आणि इंटरमॉलिक्युलर परस्परसंवाद लहान आहेत आणि U0 आणि ∆U ची मूल्ये लहान आहेत, म्हणून पॉलिमरमध्ये उत्कृष्ट गतिज आणि थर्मोडायनामिक लवचिकता आहे. उदाहरणे: PE, PP, PIB.
U0 ची मूल्ये विशेषतः पॉलिमरसाठी कमी आहेत ज्यांच्या साखळीतील एकल बॉण्डच्या पुढे दुहेरी बॉण्ड आहे.
–CH2 –CH=CH–CH2 – पॉलीब्युटाडीन समाविष्ट असलेल्या घटकांच्या मॅक्रोमोलेक्यूल्समध्ये परिचय
ध्रुवीय गट इंट्रा- आणि इंटरमॉलिक्युलर परस्परसंवाद घडवून आणतात. या प्रकरणात, ध्रुवीयतेची डिग्री लक्षणीयपणे प्रभावित करते
ध्रुवीय गट सादर करताना, लवचिकतेवर तीन संभाव्य प्रभाव आहेत:
1. ध्रुवीय गट जवळ स्थित आहेतआणि त्यांच्यामध्ये मजबूत संवाद शक्य आहे. अशा पॉलिमरच्या एका अवकाशीय स्थितीतून दुसर्या स्थानावर जाण्यासाठी मोठ्या U0 वर मात करणे आवश्यक आहे, म्हणून अशा पॉलिमरच्या साखळ्या कमीत कमी लवचिक असतात.
2. ध्रुवीय गट क्वचितच साखळीत स्थित असतातआणि त्यांच्यातील परस्परसंवाद दिसत नाहीत. U0 आणि ∆U ची मूल्ये लहान आहेत आणि पॉलिमरमध्ये गतिज आणि थर्मोडायनामिक लवचिकता जास्त आहे.

–СF 2 –СF 2 –
उदाहरण: पॉलीक्लोरोप्रीन
3. ध्रुवीय गटांची व्यवस्था केली जाते जेणेकरून विद्युत क्षेत्र एकमेकांना रद्द करतात. या प्रकरणात, मॅक्रोमोलेक्यूलचा एकूण द्विध्रुवीय क्षण शून्य असतो. म्हणून, U0 आणि ∆U ची मूल्ये कमी आहेत आणि पॉलिमरमध्ये गतिज आणि थर्मोडायनामिक लवचिकता जास्त आहे.
उदाहरण: पॉलिटेट्राफ्लुओरोइथिलीन
हेटरोचेन पॉलिमर
हेटरोचेन पॉलिमरमध्ये, C–O, C–N, Si–O आणि C–C बाँडभोवती फिरणे शक्य आहे. या बंधांसाठी U0 मूल्ये लहान आहेत आणि साखळ्यांमध्ये पुरेशी गतीशील लवचिकता आहे. उदाहरणे: पॉलिस्टर, पॉलिमाइड, पॉलीयुरेथेन, सिलिकॉन रबर.
तथापि, एच-बॉन्ड्स (उदाहरणार्थ, सेल्युलोज, पॉलिमाइड्स) तयार झाल्यामुळे हेटरोचेन पॉलिमरची लवचिकता इंटरमॉलिक्युलर परस्परसंवादाद्वारे मर्यादित असू शकते. सेल्युलोज हे कठोर चेन पॉलिमरपैकी एक आहे. यात मोठ्या संख्येने ध्रुवीय गट (–OH) आहेत आणि म्हणून सेल्युलोज इंट्रा- आणि इंटरमॉलिक्युलर परस्परसंवाद, उच्च U0 मूल्ये आणि कमी लवचिकता द्वारे दर्शविले जाते.
पॉलिमरचे आण्विक वजन. पॉलिमरचे आण्विक वजन वाढल्याने साखळी फोल्डिंग वाढते आणि त्यामुळे मोठे मॅक्रोमोलेक्यूल्स
लहान मॅक्रोमोलेक्यूल्सच्या तुलनेत जास्त गतीज लवचिकता आहे. MW जसजसे वाढते तसतसे मॅक्रोमोलेक्युल घेऊ शकणार्या कॉन्फॉर्मेशन्सची संख्या वाढते आणि साखळ्यांची लवचिकता वाढते.
अवकाशीय ग्रिड घनता. मॅक्रोमोलेक्यूल्समधील अधिक रासायनिक बंध, साखळ्यांची कमी लवचिकता, म्हणजे. अवकाशीय ग्रिडची घनता जसजशी वाढते तसतशी लवचिकता कमी होते. रेझोल मालिकेतील क्रॉसलिंक्सच्या संख्येत वाढीसह साखळी लवचिकता कमी होणे हे एक उदाहरण आहे< резитол<резит.
आकार आणि पर्यायांच्या संख्येचा प्रभाव. ध्रुवीय आणि मोठ्या घटकांच्या संख्येत वाढ झाल्यामुळे मॅक्रोमोलेक्युल युनिट्सची गतिशीलता कमी होते आणि गतीज लवचिकता कमी होते. ब्युटाडीन आणि स्टायरीनच्या कॉपॉलिमरच्या मॅक्रोमोलेक्यूल्सची लवचिकता कमी होणे आणि साखळीतील मोठ्या प्रमाणात फिनाईल घटकांची सामग्री वाढणे हे त्याचे उदाहरण आहे.
जर पॉलिमर बॅकबोनमध्ये एका कार्बन अणूवर दोन घटक असतील (उदाहरणार्थ, PMMA युनिट्समध्ये OCH3 आणि CH3), तर मॅक्रोमोलेक्युल गतीजदृष्ट्या कठोर बनते.
तापमान. वाढत्या तापमानासह, मॅक्रोमोलेक्यूलची गतिज ऊर्जा वाढते. जोपर्यंत गतीज उर्जेचे मूल्य U0 पेक्षा कमी असते, तोपर्यंत साखळी टॉर्शनल कंपने घेतात. जेव्हा मॅक्रोमोलेक्युलची गतीज उर्जा U0 मूल्याच्या बरोबरीची किंवा ओलांडते, तेव्हा दुवे फिरू लागतात. वाढत्या तापमानासह, U0 चे मूल्य थोडे बदलते, परंतु दुव्याच्या रोटेशनचा वेग वाढतो आणि गतिज लवचिकता वाढते.
प्रश्नांवर नियंत्रण ठेवा
1 पॉलिमर, संकल्पना, व्याख्या याबद्दल सामान्य माहिती.
2 परिभाषित करा आणि सेंद्रीय, गैर- उदाहरणे द्या
सेंद्रिय आणि ऑर्गेनोएलिमेंट पॉलिमर.
2 होमोचेन पॉलिमरचे वर्गीकरण, उदाहरणे.
3 हेटरोचेन पॉलिमरचे वर्गीकरण, उदाहरणे.
4 मॅक्रोमोलेक्यूल्सची थर्मोडायनामिक आणि गतिज लवचिकता. मॅक्रोमोलेक्यूल्सच्या लवचिकतेवर कोणते घटक परिणाम करतात?
5 मॅक्रोमोलेक्यूल्सचे कॉन्फिगरेशन काय आहे आणि मॅक्रोमोलेक्यूल्सच्या कॉन्फिगरेशनचे संभाव्य प्रकार कोणते आहेत? उदाहरणे.
6 मॅक्रोमोलेक्यूल्सची रचना काय आहे आणि मॅक्रोमोलेक्यूल्सची कोणत्या प्रकारची रचना शक्य आहे? उदाहरणे.
7 कोणते मापदंड आण्विक वजन दर्शवतात,पॉलिमरचे आण्विक वजन वितरण आणि पॉलीडिस्पर्सिटी?
8 ऑलिगोमर्सची आण्विक वैशिष्ट्ये.
9 पॉलिमरचे फ्रॅक्शनेशन आणि आण्विक वक्रांचे बांधकामक्यूलर वस्तुमान वितरण.
दिलेल्या कॉन्फिगरेशनमध्ये, मॅक्रोमोलेक्युलमध्ये मुख्य साखळीच्या एकल बंधांच्या अक्षाभोवती फिरण्याशी संबंधित स्वातंत्र्याच्या मोठ्या प्रमाणात अंतर्गत अंश असतात. परिणामी, मॅक्रोमोलेक्यूल विविध रूपे घेण्यास सक्षम आहे ( रचना), म्हणजे पॉलिमर रचनात्मक आयसोमेरिझम द्वारे दर्शविले जातात.
कॉन्फॉर्मेशन ही अणू आणि अणू गटांची अवकाशीय व्यवस्था आहे, जी थर्मल हालचाल आणि (किंवा) बाह्य प्रभावांच्या परिणामी मुख्य मूल्याचे रासायनिक बंध न तोडता बदलली जाऊ शकते.
खाली C-C बॉण्डभोवती 180° फिरण्याच्या परिणामी विनाइल पॉलिमरच्या आयसोटॅक्टिक ट्रायडची रचना बदलण्याच्या यंत्रणेचा एक योजनाबद्ध आकृती आहे. हे स्पष्ट आहे की अशी रचनात्मक संक्रमणे दिलेल्या कॉन्फिगरेशनमध्ये बदल आणि रासायनिक बंध तोडण्यासोबत नाहीत.
अशा प्रकारे, मॅक्रोमोलेक्यूल्सचे कॉन्फॉर्मेशनल आयसोमेरिझम पॉलिमर चेन स्ट्रक्चरच्या एकल रासायनिक बंधांभोवती अंतर्गत रोटेशनद्वारे निर्धारित केले जाते.
मॅक्रोमोलेक्यूल्सच्या कॉन्फॉर्मेशनल आयसोमेरिझमची मूलभूत तत्त्वे
कमी-आण्विक मॉडेल - 1,2-डिक्लोरोएथेनचे उदाहरण वापरून रासायनिक बंधांभोवती अंतर्गत रोटेशनच्या मूलभूत नमुन्यांचा विचार करूया.

-C-C बॉण्ड अक्षाभोवती 360° पूर्ण फिरून बाजूच्या घटकांच्या (Hi C1) परस्परसंवादामुळे, 1,2-डायक्लोरोइथेन रेणूमध्ये अनेक भिन्न रोटरी आयसोमर्स अनुक्रमे साकारले जातात, किंवा अनुरुप,विशिष्ट संभाव्य उर्जेसह. ग्राफिकदृष्ट्या, हे उर्जा नकाशाच्या रूपात दर्शविले जाऊ शकते - रोटेशन कोनावरील कॉन्फॉर्मरच्या संभाव्य उर्जेचे अवलंबन. 1,2-डिक्लोरोएथेनसाठी, समान नकाशा अंजीर मध्ये योजनाबद्धपणे दर्शविला आहे. १.३.

तांदूळ. १.३.संभाव्य ऊर्जेचे अवलंबित्व यूरोटेशन अँगलवर 1,2-डिक्लोरोइथेन रेणूचे व्हॅलेन्स-अनबॉन्डेड अणू
या प्रकारच्या रेणूंमध्ये तीन स्थिर रचना असतात: एक ट्रान्स-आणि दोन गौचे रचना (फ्रेंचमधून. गौचे- तिरकस, तिरकस), संभाव्य वक्रच्या किमानाशी संबंधित. मॅक्सिमा अस्थिर ग्रहण केलेल्या कॉन्फॉर्मेशनशी संबंधित आहे, विशेषतः r^is conformer.
पॉलिमरमध्ये, कमी आण्विक वजन असलेल्या संयुगांच्या तुलनेत सिंगल बॉन्ड्सभोवती अंतर्गत रोटेशनमध्ये अनेक विशिष्ट वैशिष्ट्ये असतात. “हेड-टू-हेड” कॉन्फिगरेशनमध्ये पॉलीव्हिनाईल क्लोराईड साखळीचा एक तुकडा विचारात घेऊ.

1,2-डिक्लोरोइथेनच्या विपरीत, पृथक तुकड्यात, दोन अणू II ऐवजी, कार्बन अणूंवरील घटक हे पॉलिमर साखळी -CH 2 - चे निरंतर आहेत. दुसऱ्या शब्दांत, gth आणि (g + 1)व्या कार्बन अणूंमधील बंधाभोवती फिरत असताना, (g + 2) वा कार्बन अणू त्यानंतरच्या साखळीच्या पुढे चालू ठेवत एक पर्यायाची भूमिका बजावतो (चित्र 1.4).

तांदूळ. १.४.
मागील बाँडच्या सापेक्ष (r + 2)व्या अणूची स्थिती शंकूच्या पायाद्वारे 0 च्या बॉण्ड कोन लक्षात घेऊन निर्दिष्ट केली जाते. तथापि, 360° चे रोटेशन केवळ तेव्हाच शक्य आहे जेव्हा अणूचे विस्तारित चालू राहते. साखळी अंतराळात फिरते, ज्यासाठी प्रचंड थर्मल उर्जा आवश्यक असते, जी नियमानुसार, रासायनिक कनेक्शनच्या पृथक्करण उर्जेपेक्षा जास्त असते. परिणामी, पॉलिमरमध्ये अंतर्गत रोटेशन होते प्रतिबंधितआणि वर्तुळाच्या एका विशिष्ट चाप मध्ये लागू केले जाते. या कमानीचा आकार ठरवतो प्रतिबंधित अंतर्गत रोटेशनचा कोन fप्रतिबंधित अंतर्गत रोटेशनच्या कोनाचे परिमाण तापमान, रासायनिक बंधाचे स्वरूप, ध्रुवीयता आणि घटकांची मात्रा, पॉलिमरची संरचनात्मक रचना इत्यादींवर अवलंबून असते.
अशा प्रकारे, पहिल्या अंदाजापर्यंत, पॉलिमर साखळीतील अंतर्गत रोटेशन मागील बॉण्डच्या सापेक्ष प्रत्येक त्यानंतरच्या बॉन्डच्या फिरण्यापर्यंत कमी केले जाते. प्रत्यक्षात, या घटनांमध्ये एक स्पष्ट सहकारी वर्ण आहे, कारण एकमेकांच्या सापेक्ष दोन शेजारच्या बंधांचे परिभ्रमण मुख्यत्वे जवळच्या वातावरणातील समान प्रक्रिया आणि लांब पल्ल्याच्या परस्परसंवादाद्वारे निर्धारित केले जाते. या संदर्भात, पॉलिमरच्या बाबतीत, प्रतिबंधित अंतर्गत रोटेशनचा कोन सरासरी मूल्य आहे. या वैशिष्ट्याचे परिमाणवाचक अंदाज खाली दिले जातील.