Når temperaturen synker, vil tettheten til elektrolytten Hvordan utjevne tettheten av elektrolytt i batteribanker? Hvis du ikke vil kjøpe en ny
Batteriet er et av hovedelementene i bilen som er ansvarlig for å starte motoren. Verdien på batteriet er vanskelig å overvurdere, fordi uten det er det umulig å starte motoren, noe som betyr at bilen ikke vil kunne bevege seg på egen hånd. Det er derfor batteriet krever spesiell oppmerksomhet til seg selv, unntatt forekomsten av ubehagelige situasjoner i form av umuligheten av å foreta en planlagt tur. Samtidig skal det bemerkes at for å opprettholde ytelsen til denne viktige strømkilden, er det ikke nødvendig å ta noen ekstra innsats, men det er nok å utføre bare et lite sett med forebyggende tiltak.
Tillatte lade- og utladningsstrømmer er lavere enn med andre teknologier. En kortslutning kan oppstå mellom de to elektrodene på grunn av veksten av dendritisk litium. Bruk av flytende elektrolytt er farlig hvis den lekker og kommer i kontakt med luft eller vann.
Bruk alltid litiumionbatterier med ekstrem forsiktighet, disse batteriene kan være eksplosive. Og som med et hvilket som helst batteri: Aldri kortslutt et batteri, vend polaritet, overbelast eller punkter dekselet. For å unngå problemer må disse batteriene alltid være utstyrt med en beskyttelseskrets, en termisk sikring og en sikkerhetsventil. De må lades med svært presise hastigheter og aldri utlades under 2,5 volt per celle.
Et blybatteri er en galvanisk celle inne i hvilken kjemisk energi omdannes til elektrisk energi som følge av pågående reaksjoner. Denne prosessen er umulig uten en elektrolytt - en syreløsning som sikrer bevegelsen av ladede partikler mellom elektrodene nedsenket i den. Som regel er elektrolytten en vandig løsning av svovelsyre med en viss tetthet. Det er en slik parameter som tettheten til elektrolytten som har en betydelig innvirkning på ytelsen til batteriet, så det må overvåkes med jevne mellomrom.
Forleng levetiden til litium-ion-batteriet. Ikke dyp utladning. Ikke oppbevar batterier for lenge uten å bruke dem. Oppbevar batteriet i romtemperatur. Hold batteriet på omtrent 40 % ladning. Ikke lad batteriet helt opp før du oppbevarer det.
Litiumklorid tionylbatteri
Ikke utlad batteriet helt før du oppbevarer det. Ikke lager reservebatterier. Når du kjøper et batteri, sjekk produksjonsdatoen, slitasjen, fra fabrikken. Ikke bruk under lading. Litium-tionylkloridparet inneholder en litiummetallanode, den letteste av metallene, assosiert med en flytende katode bestående av en porøs karbonelektrode fylt med tionylklorid.
Måling av tettheten til elektrolytten i batteriet
Det er ikke så vanskelig å måle tettheten til elektrolytten som helles i et blybatteri, men det er visse nyanser knyttet til funksjonene til enheten og prinsippet om batteriets drift. La oss liste opp noen viktige poeng som må tas i betraktning:
- Det vil være mulig å utføre tetthetsmålingsprosedyren bare i tilfelle av det såkalte betjente batteriet, som gir tilgang til banker (seksjoner) med elektrolytt gjennom fyllhull lukket med lokk. Det er gjennom disse hullene (vanligvis er antallet seks, samt antall seksjoner) at sammensetningen tas for å måle tettheten.
- I løpet av arbeidet lader og utlades bilbatteriet hele tiden. Utladningen skjer når starteren sveives, og ladningen skjer når motoren allerede går fra generatoren. Avhengig av ladningsgraden endres også elektrolyttens tetthet. Verdiene kan variere innenfor 0,15-0,16 g/cm 3 . Det er viktig å merke seg at bilgeneratoren ikke er i stand til å fullade batteriet. Ved normal drift på maskinen brukes batteripotensialet kun med 80-90 %. En full lading kan kun gis av en ekstern Lader, som definitivt må ty til før man måler tettheten til elektrolytten.
- Tettheten til en elektrolytt avhenger av temperaturen. Vanligvis utføres måling ved en temperatur på +25 °C, ellers gjøres korrigeringer.
 Anta at alle de ovennevnte forholdene er tatt i betraktning, og det er mulig å gå direkte videre til å måle tettheten. For å gjøre dette trenger du en spesiell enhet - en densimeter, som består av et hydrometer, en gummipære og et glassrør med en spiss. Enheten føres inn i batteribeholderen gjennom påfyllingshullet, og deretter suges elektrolytten inn ved hjelp av en gummipære. Det fortsetter til hydrometeret flyter. Avlesninger tas etter svingningene til hydrometerstoppet og det blir mulig å bestemme eksakt verdi. Avlesningene er tatt på en skala, mens blikket skal være på nivå med væskeoverflaten.
Anta at alle de ovennevnte forholdene er tatt i betraktning, og det er mulig å gå direkte videre til å måle tettheten. For å gjøre dette trenger du en spesiell enhet - en densimeter, som består av et hydrometer, en gummipære og et glassrør med en spiss. Enheten føres inn i batteribeholderen gjennom påfyllingshullet, og deretter suges elektrolytten inn ved hjelp av en gummipære. Det fortsetter til hydrometeret flyter. Avlesninger tas etter svingningene til hydrometerstoppet og det blir mulig å bestemme eksakt verdi. Avlesningene er tatt på en skala, mens blikket skal være på nivå med væskeoverflaten.
De kjennetegnes ved ekstremt lav selvutladning, som gir lang holdbarhet eller en levetid på 10 til 20 år. For å lette introduksjonen kan batterier utstyres med forskjellige kontakter eller settes sammen til batterier, som det finnes standardiserte versjoner av.
litium mangandioksid batteri
De bruker spiralelektroder med stor overflate for å lette leveringen av høye strømmer. Elektrolytten deres er formulert for å gi utmerket ytelse ved lave temperaturer. Vi vil ikke gå inn på tekniske detaljer av dette systemet, som i stor grad er forklart andre steder. Det er tilstrekkelig å integrere at en ionisk elektrolytt-natriumseparator bestående av beta-aluminiumoksyd tilsettes til denne temperaturbegrensningen.
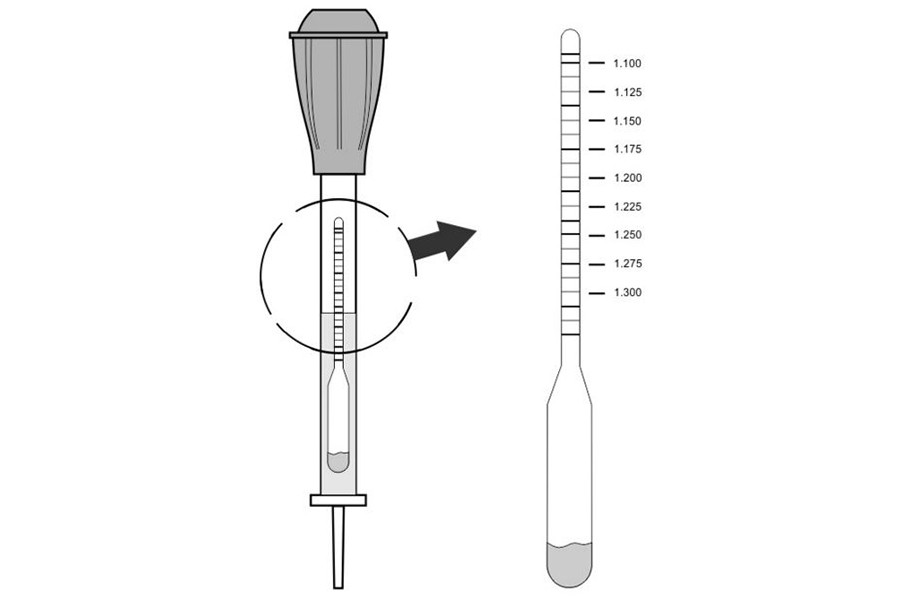 Verdien som oppnås bør ligge i området 1,25-1,27 g/cm 3 hvis bilen kjøres i midtbanen. I den kalde klimasonen (gjennomsnittlig månedlig temperatur i januar er under -15 ° C), bør indikatoren være i området 1,27-1,29 g / cm 3. Det er nødvendig å kontrollere tettheten til elektrolytten for samsvar med disse tallene i hver av de seks boksene til batteriet. Avlesningene bør ikke avvike med mer enn 0,01 g/cm3, ellers må de korrigeres.
Verdien som oppnås bør ligge i området 1,25-1,27 g/cm 3 hvis bilen kjøres i midtbanen. I den kalde klimasonen (gjennomsnittlig månedlig temperatur i januar er under -15 ° C), bør indikatoren være i området 1,27-1,29 g / cm 3. Det er nødvendig å kontrollere tettheten til elektrolytten for samsvar med disse tallene i hver av de seks boksene til batteriet. Avlesningene bør ikke avvike med mer enn 0,01 g/cm3, ellers må de korrigeres.
Dette mekanisk skjøre systemet kan være stasjonært og, hvis mulig, installeres utendørs eller i en ventilert bygning. Hver modul, som inneholder 320 sylindriske minneceller assosiert med temperatur- og sikkerhetskontrollenheter, er fylt med sand. En modul med et volum på 5,6 m3 veier mer enn 3 tonn. Fulladede batterier kan lades ut til 85 % kapasitet på omtrent 6 timer.
Den største fordelen med natrium-svovelbatterier er tilstedeværelsen av aktive materialer som ikke krever et overgangsmetall. Dette er etter min mening tre ganger for dyrt til å få et reelt gjennombrudd. Denne er mer en ny versjon har litt lavere spenning, men er tryggere, mindre giftig og billigere. Faktisk er prisen på litiumionbatterier og batterier i stor grad avhengig av materialene som brukes på katoden, som inneholder kobolt og/eller nikkel, svært dyre metaller og gjør det mer sofistikert å bruke flere kilder.
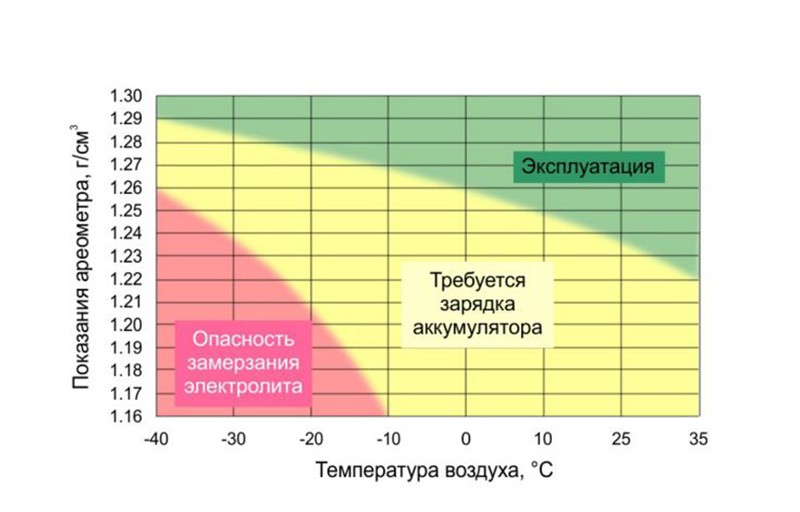
Som vi allerede har sagt, varierer tettheten til elektrolytten med temperaturen. Dette betyr at om vinteren og sommeren vil væsken i det samme fullt funksjonelle batteriet ha en annen tetthet. Tabellen nedenfor gir en ide om hvor mye avlesningene vil variere.
En annen tabell viser avhengigheten av frysepunktet til elektrolytten på dens tetthet. Basert på disse dataene er det mulig å etablere den optimale elektrolytttettheten for spesifikke klimatiske forhold. Den nedre grensen for det valgte intervallet skal sikre at elektrolytten ikke fryser selv i den mest ekstreme kulden og gir den innsatsen som kreves for å snu starteren. Samtidig er det også umulig å overvurdere tettheten, siden korrosjonsprosesser begynner å akselerere på de positive elektrodene til batteriet, noe som fører til sulfatering av platene.
Litiumbatteriet med fosfatteknologi erstatter standardkatodene med jernfosfat, et billig materiale fordi det ikke inneholder sjeldne metaller og ikke er giftig, i motsetning til kobolt. I tillegg er denne katoden veldig stabil og frigjør ikke oksygen, noe som gjør den tryggere.
For industriell utvikling i elbilen er prisreduksjon nødvendig. Det pågår imidlertid fortsatt forskning for å sikre deres levetid, bringe deres evne til andre litiumionmetoder og i det lange løp forbedre deres oppførsel ved høye temperaturer: det ser ut til at oppløsningen av jern forverrer syklingen til denne typen batterier. .
| Frysepunkt, °С | Elektrolytttetthet ved 25 °С, g/cm 3 | Frysepunkt, °С | |
|---|---|---|---|
| 1.09 | -7 | 1.22 | -40 |
| 1.10 | -8 | 1.23 | -42 |
| 1.11 | -9 | 1.24 | -50 |
| 1.12 | -10 | 1.25 | -54 |
| 1.13 | -12 | 1.26 | -58 |
| 1.14 | -14 | 1.27 | -68 |
| 1.15 | -16 | 1.28 | -74 |
| 1.16 | -18 | 1.29 | -68 |
| 1.17 | -20 | 1.30 | -66 |
| 1.18 | -22 | 1.31 | -64 |
| 1.19 | -25 | 1.32 | -57 |
| 1.20 | -28 | 1.33 | -54 |
| 1.21 | -34 | 1.40 | -37 |
Årsaker til å endre tettheten til elektrolytten
Verdiene registrert som et resultat av tetthetsmåling samsvarer ikke alltid med de nødvendige indikatorene. Avvik kan gjelde både individuelle batteribokser og alle sammen. Hvis tettheten er for høy, må du først og fremst være oppmerksom på elektrolyttnivået. Et lavt nivå er i de fleste tilfeller en konsekvens av elektrolyse, som fører til nedbrytning av vannet i elektrolytten til hydrogen og oksygen. Denne prosessen kommer til uttrykk i utseendet av bobler på overflaten av væsken, som vanligvis oppstår når batteriet lades. Hyppig "koking" kan føre til en reduksjon i konsentrasjonen av vann, og dette problemet løses ved å legge det til. Det er verdt å tilsette bare destillert vann til batteriet, mens du kontrollerer elektrolyttnivået. Vi vil snakke mer om å justere tettheten til elektrolytten nedenfor.
Denne massive energien hentet fra silisiumbasert elektrokjemi gjør at den kan tilby eksepsjonell autonomi, kraft og sikkerhet. Detaljert energi / masse 250 W / kg energi / volum 480 W / l nominell spenning per celle 3,40 volt.
Denne typen batteri er spesielt egnet for applikasjoner som krever lang batterilevetid, høy effekt og som krever flere hundre lade- og utladingssykluser, for eksempel sikkerhetssystemer eller radiokommunikasjon og andre militære bærbare systemer.
Den første fordelen med litium-svovel-modellen er at anoden vanligvis ikke består av litium, men av en silisium-karbonforbindelse. Denne tilkoblingen er betydelig mer stabil fordi den er mindre ved lading. Dette er en viktig fordel, fordi jo mer batterianoden endres, jo mer interagerer den med den flytende elektrolytten: denne prosessen får elektrolytten til å dekomponere til en gass og et fast stoff, som tørker ut batteriet. I de mest ekstreme tilfellene vokser anoden til å komme i kontakt med katoden, noe som forårsaker kortslutning og kasserer batteriet.
 Hvis alt er klart med økt tetthet, så er situasjonen noe mer komplisert med redusert tetthet. I teorien kan en av årsakene til reduksjonen i tetthet være at av en eller annen grunn har andelen svovelsyre i elektrolytten gått ned. I praksis er dette imidlertid usannsynlig, siden det i seg selv har et høyt kokepunkt, som utelukker fordampning selv ved intens oppvarming, som for eksempel oppstår ved lading batteri. En mer vanlig årsak til en reduksjon i elektrolytttettheten er den såkalte platesulfateringen, som består i dannelsen av blysulfat (PbSO4) på elektrodene. Faktisk er dette en naturlig prosess som skjer med hver batteriutlading. Men faktum er at under normal drift, etter at batteriet er utladet, må det lades (i en bil lades batteriet konstant opp fra generatoren). Ladningen er ledsaget av omvendt transformasjon av blysulfat til bly (ved katoden) og blydioksid (ved anoden) - til de aktive stoffene som danner grunnlaget for elektrodene og er direkte involvert i den kjemiske prosessen inne i batteriet. Hvis batteriet er lang tid i utladet tilstand krystalliserer blysulfat, og mister ugjenkallelig evnen til å delta i kjemiske reaksjoner. Dette er en veldig ubehagelig prosess, som et resultat av at batteriet ikke lenger kan lades helt opp selv når du bruker en ekstern lader på grunn av det faktum at ikke hele området til platene er involvert i arbeidet. Siden batteriet ikke er fulladet, gjenopprettes ikke tettheten til elektrolytten til de opprinnelige verdiene. Faktisk er det allerede en samtale om å eliminere brudd på normal funksjon av batteriet.
Hvis alt er klart med økt tetthet, så er situasjonen noe mer komplisert med redusert tetthet. I teorien kan en av årsakene til reduksjonen i tetthet være at av en eller annen grunn har andelen svovelsyre i elektrolytten gått ned. I praksis er dette imidlertid usannsynlig, siden det i seg selv har et høyt kokepunkt, som utelukker fordampning selv ved intens oppvarming, som for eksempel oppstår ved lading batteri. En mer vanlig årsak til en reduksjon i elektrolytttettheten er den såkalte platesulfateringen, som består i dannelsen av blysulfat (PbSO4) på elektrodene. Faktisk er dette en naturlig prosess som skjer med hver batteriutlading. Men faktum er at under normal drift, etter at batteriet er utladet, må det lades (i en bil lades batteriet konstant opp fra generatoren). Ladningen er ledsaget av omvendt transformasjon av blysulfat til bly (ved katoden) og blydioksid (ved anoden) - til de aktive stoffene som danner grunnlaget for elektrodene og er direkte involvert i den kjemiske prosessen inne i batteriet. Hvis batteriet er lang tid i utladet tilstand krystalliserer blysulfat, og mister ugjenkallelig evnen til å delta i kjemiske reaksjoner. Dette er en veldig ubehagelig prosess, som et resultat av at batteriet ikke lenger kan lades helt opp selv når du bruker en ekstern lader på grunn av det faktum at ikke hele området til platene er involvert i arbeidet. Siden batteriet ikke er fulladet, gjenopprettes ikke tettheten til elektrolytten til de opprinnelige verdiene. Faktisk er det allerede en samtale om å eliminere brudd på normal funksjon av batteriet.
Sølv aluminiumoksid batteri
Svovel samhandler også med den flytende elektrolytten, noe som reduserer ytelsen til batteriene til de mister sine full kraft. Sølv-sink-paret brukes til å lage primære eller sekundære batterier. I primære battericeller består anoden av sink og en sølvoksidkatode. I sekundære battericeller er anoden laget av sinkoksid og en sølvkatode. I alle tilfeller er elektrolytten basert på kaliumklorid.
Detaljerte hovedapplikasjoner Militær veiledningstorpedoer, pilotering, aktivering av Ariana oppladbare batterier brukes til fysiske aktiviteter. Av sikkerhets- og ytelsesgrunner aktiveres batteriet kun i siste øyeblikk ved elektrolyttinnsprøytning. Sølv-sink-batterier utmerker seg ved sin energitetthet og kraft.
Delvis sulfatering av platene kan elimineres ved hjelp av kontroll- og treningssykluser, som består i å lade og deretter utlade batteriet til et visst nivå. De fleste moderne ladere har denne funksjonen, så det er fornuftig å bruke den, spesielt hvis batteriet har vært i utladet tilstand av en eller annen grunn. Desulfateringsprosedyren er veldig lang og kan ta opptil flere dager. Hvis det ikke ga resultater, er et ekstremt tiltak å øke tettheten ved å tilsette en korrigerende elektrolytt (densiteten er ca. 1,40 g/cm3). Denne metoden kan bare betraktes som en midlertidig løsning på problemet, fordi årsaken som sådan ikke er eliminert.
Sølv magnesiumklorid batteri
Detaljert energivekt 3 W/k Energivolum 103 W/L Levetid 3 til 5 år Antall ladesykluser 300 til 900 Merkespenning per celle 9 til 1 volt. Denne teknologien bruker tynt ark bor-silikatfiber mellom blyplatene til batteriet. Dette tynne arket er impregnert med en elektrolytt som kommer i kontakt med platene.
Disse batteriene har samme kvaliteter som gelbatterier og tillater flere feil prosess. Siden elektrolytten er impregnert med fiber, kan den ikke synke selv om batterikassen går i stykker, så transporten er mye enklere og sikrere.
Hvordan øke tettheten til elektrolytten
Det er mulig å senke eller øke tettheten til elektrolytten i batteriet ved å pumpe ut en viss mengde av den, og tilsette destillert vann eller en elektrolytt med økt tetthet (korrigerende) i stedet. Denne prosedyren er tidkrevende, siden pumpe-påfyllingssyklusen kan gjentas flere ganger til ønsket verdi er nådd. Etter hver justering må du sette batteriet på lading (minst 30 minutter), og deretter la det stå (0,5-2 timer). Disse handlingene er nødvendige for bedre blanding av elektrolytten og utjevning av tettheten i glassene.
Gassfasen under batterilading overfører oksygen til de negative platene for å gjøre det om til vann, og unngår dermed vanntap. Denne handlingen er mer enn 99 % effektiv, noe som gjør vanntapet ubetydelig. Dette fenomenet gir en høy grad fleksibilitet i kostnader og utgifter.
Denne lave hastigheten gir mulighet for lange perioder med lagring uten hyppig lading som med standard batterier. Ved alvorlig overbelastning er hydrogenutslippet under 4 %, noe som er i tråd med strenge luftfartsstandarder og trange rom.
I prosessen med å heve (eller senke) tettheten til elektrolytten, bør man ikke glemme å kontrollere nivået. Det utføres av et glassrør med to hull langs kantene. Den ene kanten er nedsenket i elektrolytten til den treffer sikkerhetsnettet. Deretter lukkes den øvre enden med en finger, og selve røret løftes forsiktig sammen med en væskekolonne inni. Høyden på denne kolonnen indikerer avstanden fra den øvre kanten av platene til overflaten av den fylte elektrolytten. Den skal være 10-15 mm. Hvis batteriet har en indikator (rør) eller et gjennomsiktig etui med minimums- og maksimumsmerker, er det mye lettere å kontrollere nivået.
De har den høyeste energitettheten av ethvert batteri, men de er ikke mye brukt på grunn av kostnader, holdbarhet, oppstartstid og problemer med biprodukter som har begrenset dem til hovedsakelig militære applikasjoner. elektrisk bil med aluminiumsbatterier kunne ha ti til femten ganger så mange bly-syre-batterier med mye mindre totalvekt. Når aluminiumanoden er forbrukt av reaksjonen til atmosfærisk oksygen på katoden nedsenket i elektrolytten for vannbasert, til den hydrerte formen av alumina, vil batteriet ikke lenger produsere elektrisitet.
Ikke glem at alle operasjoner med elektrolytt må utføres nøye, med vernehansker og vernebriller.
Periodisitet
Kontroller nivået og tettheten til elektrolytten hver 15.000 km.
Det er imidlertid mulig å lade opp batteriet mekanisk med nye aluminiumanoder laget av resirkulert hydratisert alumina. Faktisk vil resirkulering av generert alumina være viktig hvis luftbatterier av aluminium er mye brukt. Disse reaksjonene skaper en potensialforskjell på 2 volt.
Det er imidlertid fortsatt noen tekniske problemer som må løses for å gjøre luftbatterier egnet for elektriske kjøretøy. Rene aluminiumanoder korroderes av elektrolytten, så aluminium er vanligvis legert med tinn eller andre proprietære elementer. Hydratisert alumina, som dannes ved reaksjonen av celler, danner et kolloidalt stoff ved anoden og reduserer produksjonen av elektrisitet. For eksempel er det utviklet tilsetningsstoffer som danner alumina som et pulver i stedet for en gel.
Rengjør batteriet regelmessig for støv og skitt. Hvis toppdekselet er sprukket eller buler, skift ut batteriet.
Elektrolytten må være gjennomsiktig. En brun nyanse indikerer utskillelse av den aktive massen til platene - batteriet må byttes.
Advarsler
Under drift avtar elektrolyttnivået gradvis på grunn av fordampning av vann, som er en del av det. For å gjenopprette nivået, tilsett bare destillert vann til batteriet.
I tillegg har legeringene vist seg å danne mindre gel enn rent aluminium. Disse katodene fungerer bra, men de kan være dyre. Disse batteriene har blitt brukt som reservebatterier i flere telefonsentraler som reservestrømkilde.
For bærbare datamaskiner og mobiltelefoner luftkjølte batterier brukes og er konstruert for slik bruk. Detaljert energivekt 370 W / k nominell spenning av celler fra 35 til 65 volt. Sink-luft-batterier og sink-luft brenselceller, elektrokjemiske batterier drevet av oksidasjon av sink med atmosfærisk oksygen. Disse batteriene har høy energitetthet og er relativt rimelige å produsere. De brukes i høreapparater og eksperimentelle elektriske kjøretøy.
Når du sjekker tettheten, vær forsiktig: elektrolytten inneholder svovelsyre! Elektrolyttdråper som har falt på deler av bilen eller på åpne områder av kroppen, skyll umiddelbart med mye vann.
Ikke røyk eller bruk åpen ild mens du lader batteriet.
Før lading, fjern batteriet fra bilen, ellers kan den "kokte" elektrolytten sprute ut på karosseriet og deler av bilen.
De kan være viktig del fremtidig sinkøkonomi. Oksydasjonen av sink i sinkoksid og vann føres tilbake til systemet. Vannet og hydroksylene til anoden gjenbrukes ved katoden, så vanntilførselen fungerer kun som en katalysator. Reaksjoner gir maksimalt nivå 65 volt, men dette reduseres til 4-35 volt ved å redusere luftstrømmen i cellen, dette gjøres vanligvis slik at høreapparatbatterier reduserer hastigheten på vanntørkingen.
Brenselcelle sink-luft-begrensning refererer generelt til et sink-luft-batteri der sink-drivstoffet er i nivå og tapet av sinkoksid fjernes uten avbrudd. Dette oppnås ved å skyve elektrolyttpastaen eller sinkgranulene inn i anodekammeret. Sinkkoagulumoksid pumpes inn i en fleksibel eller avfallstank inne i drivstofftanken, og pasta eller ferske sinkgranulat tas fra drivstofftanken. Sinkoksidtap pumpes ut ved drivstoffpåfyllingsstasjoner og sendes til et gjenvinningsanlegg.
Tabell 1. Korreksjon av elektrolytttetthet avhengig av
temperatur
| Elektrolytttemperatur, °С |
Tillegg, g/cm 3 |
|
-40 til -26 |
|
|
-25 til -11 |
|
|
-10 til +4 |
|
|
+5 til +19 |
|
|
+20 til +30 |
|
|
+31 til +45 |
Tabell 2. Elektrolytttetthet ved 25 °С, g/cm 3
|
Klimaområde (gjennomsnittlig månedlig lufttemperatur i januar, °С) |
Årstid |
Fulladet batteri |
Batteriet er ladet |
|
|
Veldig kaldt |
Vinter |
|||
|
Kald |
Hele året |
|||
|
Moderat |
Hele året |
|||
|
varmt fuktig |
Hele året |
|||
|
varm tørr |
Hele året |
|||
Tabell 3. Omtrentlig normer for justering av tettheten til elektrolytten
|
Nødvendig elektrolytttetthet i batteriet, g/cm 3 |
||||
|
Reell elektrolytttetthet, g/cm 3 |
Volumet av elektrolytt fjernet fra batteriet, cm 3 |
|||
FREMGANGSMÅTE
|
||||||||||||||||||||||||||||